은 산화물 (Ag2O) 구조, 특성, 명명법 및 용도
그 은 산화물 화학식이 Ag 인 무기 화합물2O. 원자를 하나로 묶는 힘은 전적으로 이온 성질이다. 그러므로 그것은 2 개의 Ag 양이온의 비율이 존재하는 이온 성 고체로 구성된다+ 음이온과 정전 기적으로 상호 작용 O2-.
산화물 음이온, O2-, 그것은 표면의은 원자가 환경의 산소와 상호 작용함으로써 생겨난 다. 철 및 기타 많은 금속과 매우 유사한 방식으로 붉은 조각과 녹슬지 않는은 조각이나 보석은은 산화물의 특징 인 흑색으로 변합니다..

예를 들어 위의 이미지에서 녹슨은 컵을 볼 수 있습니다. 그것의 검게 한 표면을주의하십시오, 아직도 장식적인 광택을 유지하더라도; 녹슨 은색 물체조차도 장식 용도로 충분히 매력적이라고 간주 될 수 있습니다..
산화은의 성질은 처음에는 원래의 금속 표면을 망치지 않는다. 이것은 공기 중의 산소와의 간단한 접촉에 의해 실온에서 형성된다; 더 흥미로운 것은 고온 (200 ° C 이상)에서 분해 될 수 있으며,.
즉, 이미지의 유리를 잡고 열이 강한 열을 가하면 은빛의 빛을 되 찾을 수 있습니다. 그러므로, 그 형성은 열역학적으로 가역적 인 과정이다.
은 산화물은 또한 다른 특성을 가지고 있으며, 단순한 Ag 공식2또는 복잡한 구조 조직과 풍부한 다양한 솔리드를 포함합니다. 그러나, Ag2아니면 아마도 Ag 옆에 있을까요?2O3, 가장 대표적인은 산화물.
색인
- 1은 산화물의 구조
- 1.1 발렌시아 수의 변화
- 2 물리 화학적 특성
- 2.1 분자량
- 2.2 외관
- 2.3 밀도
- 2.4 융점
- 2.5 Kps
- 2.6 용해도
- 2.7 공유 특성
- 2.8 분해
- 3 명칭
- 3.1 발렌시아 I 및 III
- 3.2 복합은 산화물에 대한 체계적인 명명법
- 4 용도
- 5 참고
은 산화물의 구조
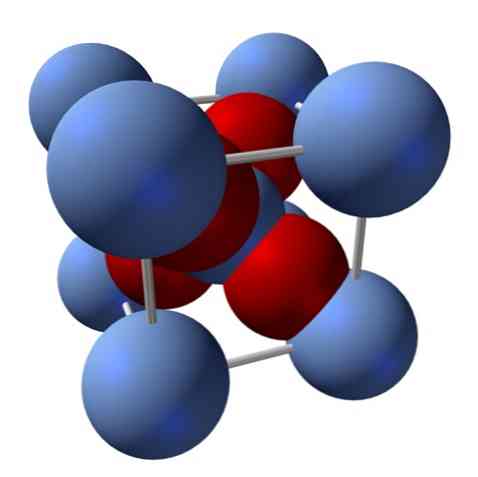
그것의 구조는 어떻습니까? 처음에 언급했듯이 이온 성 고체입니다. 이러한 이유 때문에, 그 구조 내에 Ag-O 또는 Ag = O 공유 결합이 존재할 수 없다. 왜냐하면 존재한다면,이 산화물의 성질이 크게 바뀔 것이기 때문입니다. 그런 다음 Ag 이온+ 와 O2- 2 : 1의 비율 및 정전 인력.
은 산화물의 구조는 이온 힘이 우주에서 Ag 이온을 처분하는 방식에 의해 결정된다+ 와 O2-.
예를 들어 상단 이미지에서 입방 결정 시스템을위한 단위 셀, 즉 Ag 양이온+ 은색 구가 있고, O2- 붉은 구체.
구의 수를 세면, 한 눈에 은빛 파랑과 네 가지 색이 9 개 있다는 것을 알 수 있습니다. 그러나 큐브 안에 포함 된 구체의 단편 만 고려됩니다. 이들을 계수하는 것은 전체 구체의 분율이므로 Ag의 2 : 1 비율을 만족해야합니다2O.
AgO 4 면체의 구조 단위 반복4 다른 4 명의 Ag에 둘러싸여있다.+, 모든 흑색 고체가 만들어집니다 (이 크리스탈 배치가 가질 수있는 틈이나 불규칙성을 없앱니다).
발렌시아 수의 변화
지금 AgO 4 면체에 집중하지 않음4 AgOAg (상단 입방체의 꼭지점을 관찰) 라인에서,은 산화물 고체는 다른 관점에서, (기울어졌지만) 선형으로 배열 된 다중 이온층으로 구성 될 것이다. 이 모든 것은 Ag 주변의 "분자"기하학의 결과로서+.
위의 내용은 이온 구조에 대한 여러 연구에 의해 입증되었습니다..
은이 전자를 잃을 때 전자 구성이 [Kr] 4d이기 때문에 은은 원자가 +1로 주로 작용합니다.10, 매우 안정적입니다. Ag와 같은 다른 원자가2+ 및 Ag3+ 그들은 거의 완전하게 채워진 궤도로부터 전자를 잃어 버리기 때문에 덜 안정하다..
Ag 이온3+, 그러나, Ag에 비해 상대적으로 덜 불안정하다2+. 사실 그것은 Ag 회사와 공존 할 수 있습니다.+ 구조를 화학적으로 풍부하게 함.
전자 구성은 [Kr] 4d입니다.8, 짝이없는 전자와 함께 안정성을 제공한다..
Ag 이온 주위의 선형 구조와 달리+, Ag 이온의 경우3+ 그것은 사각형 평면입니다. 따라서, Ag 이온을 갖는은 산화물3+ AgO 사각형으로 구성된 레이어로 구성됩니다.4 (사면체가 아닌) AgOAg 라인에 의해 정전 기적으로 연결됨; Ag의 경우4O4 Ag2O ∙ Ag2O3 단사 구조의.
물리 화학적 특성

당신이 주 이미지의 은색 컵의 표면을 긁으면 검은 색 일뿐 아니라 갈색 또는 갈색 색조 (상단 이미지)를 가진 단색을 얻을 수 있습니다. 순간적으로보고 된 물리적 및 화학적 특성 중 일부는 다음과 같습니다.
분자량
231,735 g / mol
외관
분말 형태의 흑색 고체 (이온 성 고체 임에도 불구하고 결정 성 외관이 없음). 그것은 무취이며 물과 혼합되어 금속성 맛을냅니다.
밀도
7.14 g / mL.
융점
277-300 ℃. 확실하게, 그것은 단단한은으로 녹습니다; 즉, 액체 산화물을 형성하기 전에 부서지기 쉽다..
Kps
1.52 ∙ 10-8 20 ℃의 물에서 따라서 물에 거의 용해되지 않는 화합물입니다.
용해도
그 구조의 이미지를주의 깊게 본다면, Ag의 구체2+ 와 O2- 그들은 거의 크기에 동의하지 않습니다. 결과적으로, 작은 분자 만이 결정 성 격자의 내부로 침투 할 수 있고, 거의 모든 용매에서 불용성이된다. 염기와 산과 같이 반응하는 것을 제외하고는.
공유 문자
반복적으로 산화은이 이온 성 화합물이라고 말했지만 저 융점과 같은 특정 성질은이 주장과 모순된다..
확실히, 공유 적 특성의 고려는 그 구조에 대해 설명 된 것을 무너 뜨리지는 않는다. Ag의 구조에 그것을 덧붙이면 충분할 것이다.2또는 공유 결합을 나타내는 구 및 막대의 모델.
또한, 사면체 및 사각형 평면 AgO4, AgOAg 계통뿐만 아니라 공유 결합 (또는 공유 결합 이온 결합)으로 연결될 수있다.
이를 염두에두고 Ag2또는 실제로 폴리머 일 것입니다. 그러나 공유 성질을 가진 이온 성 고체로 간주하는 것이 좋습니다 (링크 성질은 오늘날에도 여전히 과제입니다).
분해
처음에는 그 형성이 열역학적으로 가역적이어서 열을 흡수하여 금속 상태로 되돌아 간다는 언급이있었습니다. 이 모든 것은 그러한 반응에 대한 두 가지 화학 반응식으로 나타낼 수 있습니다.
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2Ag2O (s) + Q => 4Ag (s) + O2(g)
여기서 Q는 방정식의 열을 나타냅니다. 이것은 왜 녹슨은 컵의 표면을 태우는 불빛이 은빛 빛을내는지를 설명합니다..
그러므로 Ag가 있다고 가정하는 것은 어렵다.2O (l) 그것은 열에 의해 즉시 분해 될 것이기 때문에; 압력이 너무 높아서 상기 갈색의 검은 색 액체를 얻을 수 없다면.
명명법
Ag 이온의 가능성이 도입되었을 때2+ 및 Ag3+ 공통적이고 우세한 Ag+, 용어 '은 산화물'은 Ag를 언급하기에는 불충분 해 보인다.2O.
이것은 Ag 이온+ 다른 것들보다 더 풍부하여, Ag가 취해진 다.2아니면 유일한 산화물로; 어느 것이 정확하지 않다..
Ag를 고려한다면2+ 그것의 불안정성을 고려할 때 실제적으로 존재하지 않는 것처럼, 원자가 +1과 +3 인 이온 만 존재할 것이다. 즉, Ag (I) 및 Ag (III).
발렌시아 I 및 III
가장 작은 원자가 Ag (I)이기 때문에 이름에 접미어 -oso를 추가하여 이름을 붙입니다. 아 젠트 룸. 그래서, Ag2또는 : argentoso oxide 또는 체계적인 명명법에 따라, diplata monoxide.
Ag (III)가 완전히 무시된다면, 그 전통적인 명명법은 다음과 같아야한다 : 아르헨티나 산화물 대신은 산화물.
반면에 더 큰 원자가 인 Ag (III)는 그 이름 앞에 -ico가 붙습니다. 그래서, Ag2O3 은 산화은 (2 Ag 이온)3+ 3 개의 O가있는2-). 또한, 체계적인 명명법에 따른 그 이름은 : diplata trioxide.
Ag의 구조가 관찰되면2O3, 오존에 의한 산화 생성물이라고 추정 할 수있다.3, 산소 대신. 따라서 공유 결합 성은 Ag-O-O-O-Ag 또는 Ag-O 결합과의 공유 결합 화합물이므로 더 커야한다.3-Ag.
복합은 산화물의 체계적인 명명법
AgO는 Ag라고도 쓰며4O4 Ag2O ∙ Ag2O3, 그것은 +1과 +3의 원자가를 가지고 있기 때문에은 산화물 (I, III)이다. 체계적인 명명법에 따른 그것의 이름은 다음과 같다 : tetraplate fouroxide.
이 명명법은 다른 화학 양 론적으로 더 복잡한은 산화물을 다룰 때 큰 도움이됩니다. 예를 들어, 2 개의 고형물 2Ag2O ∙ Ag2O3 및 Ag2O ∙ 3Ag2O3.
첫 번째 방법을보다 적절한 방법으로 작성하는 것은 다음과 같습니다. Ag6O5 (Ag와 O의 원자 수를 세고 더한다). 그의 이름은 헥사 플레이트 오산화입니다. 이 산화물은 Ag보다 덜 풍부한은 조성을 갖는다는 것을 주목하라.2O (6 : 5 < 2:1).
그렇지 않으면 두 번째 솔리드를 작성하는 동안 다음과 같이됩니다. Ag8O10. 그 이름은 octaplate decaoxide (8 : 10 또는 4 : 5 비율)입니다. 이 가설적인은 산화물은 "매우 산화 됨".
용도
은 산화물에 대한 새롭고 정교한 용도의 연구는 오늘날에도 여전히 수행되고 있습니다. 그 중 일부는 다음과 같습니다 :
-그것은 암모니아, 질산 암모늄 및 물에 용해되어 Tollens 시약을 형성합니다. 이 시약은 유기 화학 연구소 내 정성 분석에 유용한 도구입니다. 그것은 시료에서 알데히드의 존재를 결정할 수있게하며, 긍정적 인 응답은 시험관에서 "은 거울 (silver mirror)"을 형성하는 것입니다.
-금속 아연과 함께 실버 아연 산화물의 기본 배터리를 형성합니다. 이것은 아마도 가장 흔하고 가정적인 용도 중 하나 일 것입니다.
-그것은 예를 들어 CO를 흡수하는 가스 정제기의 역할을한다.2. 데워지면 가스가 방출되어 여러 번 재사용 할 수 있습니다..
-은의 항균성 때문에 그 산화물은 생물 분석 및 토양 정화 연구에 유용합니다..
-그것은 알데히드를 카르 복실 산으로 산화시킬 수있는 약한 산화제입니다. 그것은 또한 호프만 반응 (3 차 아민)에서 사용되고 시약 또는 촉매로서 다른 유기 반응에 참여합니다.
참고 문헌
- Bergstresser M. (2018). 은 산화물 : 포뮬라, 분해 및 형성. 공부해라. 원본 주소
- III / 17E-17F-41C 권의 저자 및 편집자. (s.f.). 은 산화물 (Ag (x) O (y)) 결정 구조, 격자 파라미터. (과학 기술의 수치 적 자료와 기능적 관계), 41 권. Springer, Berlin, Heidelberg.
- 마헨드라 쿠마르 Trivedi, 라마 모한 Tallapragada, 앨리스 Branton, Dahryn Trivedi, 고팔 나약, Omprakash Latiyal, Snehasis 자나. (2015). 실버 산화물 분말의 물리적 및 열적 특성에 에너지 Biofield 치료의 잠재적 영향. 의 생명 과학 및 공학 국제 저널. Vol. 3, No. 5, pp. 62-68. 도이 : 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). 은 산화물의 분해. 오레곤 대학 원본 주소 'chemdemos.uoregon.edu'
- 부싯돌, Deyanda. (2014 년 4 월 24 일). 은 산화물 배터리의 사용. Sciencing. 원본 주소 'sciencing.com'
- Salman Montasir E. (2016). UVVisible 분광 광도계를 이용한은 산화물 (Ag2o)의 일부 광학 특성 연구. [PDF] 원본 주소 'iosrjournals.org'
- Bard Allen J. (1985). 수용액의 표준 전위. Marcel Dekker. 검색자 : books.google.co.ve


