수소화 나트륨 (NaH) 특성, 반응성, 위험 및 용도
그 수소화 나트륨 화학식 NaH의 무기 화합물이다. 나트륨과 수소 화합물 사이에는 이온 결합이있다. 그 구조는 그림 1에 나와 있습니다. 이것은 소금물과 유사한 수 소화물 인 Na +와 H- 이온으로 구성된 보리 인, 메탄, 암모니아와 같은 분자 수소화 물과는 대조적으로 염분 하이드 라이드를 대표합니다 와 물.
결정 구조는 팔면체 형상을 제시 각 분자는 수소화 나트륨 이온 (8)에 의해 둘러싸여 있으며, 상기 배위 수가 6을 갖고도 2에 도시되어있다 (표 동계 [셰필드 주 대학과 WebElements, 1993년에서 2016년까지).
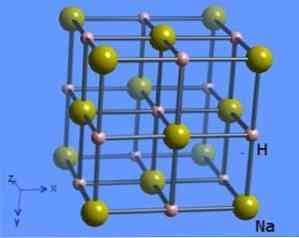
이 화합물은 다음과 같이 나트륨과 수소 가스 (나트륨 하이드 라이드 화학식 - 수소화 나트륨 용도, 특성, 구조 및 화학식, 2005-2017) 사이의 직접 반응에 의해 제조됩니다 :
H2 + 2Na → 2NaH
수소화 나트륨이 안전 취급 광유 (중량 백분율 중량) W / W 분산액의 형태로 상업적으로 60 % 판매 (수소화 나트륨, N.D.).
색인
- 1 수소화 나트륨의 물리 화학적 특성
- 2 반응성 및 위험성
- 3 용도
- 4 참고
수소화 나트륨의 물리 화학적 특성
수소화 나트륨은 일반적으로 회색이나 은색으로 얻어 지지만 순수 할 때 흰색 고체이다. 그 모양은 그림 3에 나와있다..

NaH는 23.99771 g / mol의 분자량, 1.396 g / ml의 밀도 및 800 ℃의 융점을 갖는다 (Royal Society of Chemistry, 2015). 그것은 암모니아, 벤젠, 사염화탄소 및 이황화 탄소에 불용성이다 (National Center for Biotechnology Information, s.f.).
이 화합물은 매우 불안정합니다. 순수한 NaH는 공기 중에 쉽게 발화 할 수 있습니다. 대기 중에 존재하는 물과 접촉하면 가연성이 높은 수소를 방출합니다.
공기와 습기에 노출 될 때, NaH는 또한 반응에 따라 수산화 나트륨 (NaOH)의 강력한 부식성 염기로 쉽게 가수 분해됩니다 :
NaH + H2O → NaOH + H2
이 반응에서 수소화 나트륨은 염기처럼 행동 함을 알 수있다. 이것은 전기 음성도 때문입니다..
나트륨은 전기 음성도를 갖는 상당히 낮은 (≈1,0) 수소 나트륨 양이온 및 음이온을 생성하기 위해 자체적으로 멀리 나트륨으로부터 전자 밀도를 추출한 것을 의미 수소 (≈2,1)보다 수 소화물.
화합물이 브 st스 테드 산이 되려면 수소와 전자 밀도를 분리해야하는데, 즉 산소, 불소, 질소 등과 같은 전기 음성 원자에 연결해야합니다. 그런 다음에 만 공식적으로 H +로 기술 될 수 있으며 그러한 것으로 분리 될 수 있습니까?.
수 소화물은 H-로 더 잘 묘사되고 자유 전자 쌍을 가지고 있습니다. 따라서, 그것은 브 st스 테드 염기가 아니고 산성입니다. 사실, 브 st스 테드 산 / 염기 정의를 루이스의 방식대로 확장하면 나트륨 (Na +)이 여기의 산성 종이라는 결론에 도달하게됩니다.
H- 염기와 H + 산의 브 st스 테드 산 / 염기 반응 생성물은 H2가된다. 산성 수소는 물에서 직접 추출되기 때문에 수소 기체가 거품을 일으킬 수있어 반응이 열역학적으로 유리하지 않더라도 평형을 대체 할 수 있습니다.
나머지 Na + 양이온으로 써서 수산화 나트륨을 얻을 수있는 OH- 이온을 남겨 둘 수 있습니다 (왜 물과 반응 할 때 고체상의 수소화 나트륨을 사용하고 산을 사용하지 않습니까?, 2016).
반응성 및 위험성
이 화합물은 강력한 환원제입니다. 유리에 SiO2를 공격합니다. HF, HCl, HBr 및 HI를 형성하기 위해 수분이 존재할 때 가스 F2, Cl2, Br2 및 I2 (후자 인 100 ° C 이상의 온도에서)와 접촉시 점화됩니다.
황과 반응하여 Na2S와 H2S를 생성합니다. 그것은 디메틸 sulfoxide와 폭발적으로 반응 할 수 있습니다. -60 ° C조차 아세틸렌과 격렬하게 반응합니다. 그것은 불소가 자발적으로 가연성입니다..
에스테르가 격렬하게 분해되도록 에틸 -2,2,3- 트리 플루오로 프로 피오 네이트에서 중합 반응을 개시한다. 석시 네이트와 에틸 트리 플루오로 아세테이트의 반응에서의 존재는 폭발을 일으켰다 (SODIUM HYDRIDE, 2016).
수소화 나트륨은 물과의 부식 부산물로 인해 피부 또는 눈에 부식성이있는 것으로 간주됩니다.
눈에 닿은 경우에는 다량의 물로 눈꺼풀 아래 최소한 15 분 동안 씻어야하며 즉시 의사에게 진찰을 받아야합니다..
피부에 닿았을 경우 즉시 닦고 물로 헹구십시오. 자극이 지속되면 의료 조치를 취하십시오..
물에 대한 반응으로 인하여 섭취하면 유해합니다. 구토를 유도하지 마십시오. 즉시 의료 조치를 취하여 피해자를 의료 센터로 이송해야합니다..
기름에 수소화 나트륨의 분산은 먼지가 아닙니다. 그러나 반응하는 물질은 미세한 부식성 미스트를 방출 할 수 있습니다. 흡입의 경우, 입을 물로 헹구고 희생자를 신선한 공기가있는 곳으로 옮기십시오. 의학적주의가 요구되어야한다 (Rhom and Hass Inc., 2007).
용도
수소화 나트륨의 주된 용도는 탄소 음이온의 생성을 통해 발생하는 축합 및 알킬화 반응을 수행하는 것이다 (염기에 의해 촉매 됨).
오일 중 수소화 나트륨은 아세토 에스테르, 클라 이젠 축합, Stobbe, 디크과 관련된 반응의 탈 양자화 화제로서 기능 할 수 있다는 나트륨 알코올 레이트 및 나트륨 금속을 닮았다. 다른 응축제보다 다음과 같은 장점이 있습니다.
- 더 강한 기초가되어 더 직접적인 탈 양자화가 일어난다..
- 초과가 필요하지 않습니다..
- 생성 된 H2는 반응의 정도를 측정합니다.
- 감소와 같은 2 차 반응은 제거됩니다..
2- 아미노 피리딘 및 페 노티 아진과 같은 방향족 및 헤테로 사이 클릭 아민의 알킬화는 톨루엔 - 메틸 포름 아미드의 혼합물을 사용하여 높은 수율로 용이하게 달성된다. 디메틸 포름 아미드의 농도는 반응 속도를 제어하는 변수이다 (HINCKLEY, 1957).
이 연료 전지 차량에 사용하는 수소 저장 용 수소화 나트륨의 사용이 제안되어 있으며, 수 소화물 수소를 방출하는 물의 존재 플라스틱 과립으로 분쇄 동봉 되.
참고 문헌
- HINCKLEY, M. D. (1957). 수소화 나트륨의 제조, 취급 및 사용. Advances in Chemistry, 19 권, 106-117 쪽.
- Mark Winter [University of Sheffield and WebElements Ltd, U. (1993-2016)). 나트륨 : 수소화 나트륨. WebElements에서 검색 : webelements.com.
- 생명 공학 정보 센터. (s.f.). PubChem 복합 데이터베이스; CID = 24758. PubChem에서 검색 됨 : pubchem.ncbi.nlm.nih.gov.
- Rhom과 Hass inc. (2007, 12 월). 석유의 60 % 수소화 나트륨. dow.com에서 가져온.
- 화학 왕립 학회. (2015). 수소화 나트륨. ChemSpider에서 가져온 항목 : chemspider.com.
- 소듐 하이드 라이드. (2016). cameochemicals에서 검색 : cameochemicals.noaa.gov.
- 나트륨 수 소화물 공식 - 나트륨 수 소화물 용도, 특성, 구조 및 공식. (2005-2017). Softschools.com에서 검색 함 : softschools.com.
- 소듐 하이드 라이드. (s.f.). chemicalland21에서 가져온 : chemicalland21.com.
- 물과 반응 할 때 고체 수소화 나트륨은 왜 산성이 아닌가? (2016, 4 월 20 일). stackexchange에서 검색 : chemistry.stackexchange.com.


