아세트산 나트륨 수식, 준비, 속성, 위험 및 용도
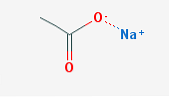
그 나트륨 아세테이트, 나트륨 에타 노 에이트 (sodium ethanoate, 약칭 NaOAc)는 아세트산의 나트륨 염입니다. 그것의 화학 공식은 CH3COONa 및 나트륨 이온과 아세테이트 이온 사이에 이온 결합을 갖는다.
이 화합물은 식물과 동물의 조직에 자연적으로 존재합니다. 그것은 무수 또는 삼수 처리 된 어떤 형태로든 발견 될 수 있습니다. 두 이온, Na + 및 CH3COO- 는 유기체에 존재하며 필수 기능을 수행합니다 : 총 체내 수분의 조절 자로서의 나트륨 이온 및 수소 수용체로서의 아세테이트 이온 (나트륨 아세테이트 수식, 2005-2017).
색인
- 1 준비
- 2 물리 화학적 특성
- 3 반응성 및 위험성
- 4 취급 및 저장 방법
- 5 용도와 용도
- 6 참고 문헌
준비
나트륨 아세테이트는 누구에게나 쉽고 간편하게 준비 할 수있는 화합물입니다. 결정화가 고체 상태의 물과 닮았 기 때문에 일반적으로 그 준비는 "뜨거운 얼음 실험"으로 알려져있다 (과학자, 2016).
초산 나트륨을 준비하려면 식초 (초산)와 탄산나트륨 또는 중탄산 나트륨 만 있으면됩니다. 식초에 중탄산염을 넣으면 반응에 따라 이산화탄소가 배출되므로 발포 반응을 일으 킵니다..
CH3COOH + NaHCO3 → CH3COONa + H2콜로라도 주3
H2콜로라도 주3 → CO2 + H2O
중탄산염 또는 중탄산 나트륨은 나트륨 아세테이트와 물이 반응에 따라 생산되는 수산화 나트륨 (잿물)으로 대체 될 수있다 :
CH3COOH + NaOH → CH3COONa + H2O
이 반응은 비등을 일으키지 않지만, 수산화 나트륨은 중탄산염보다 다루기가 더 어렵다는 단점이있다.
결정화 (또는 뜨거운 얼음의 효과) 효과를 얻기 위해서는 중탄산염을 과잉으로 용해시키기 위해 용액을 가열하여 과포화시켜야합니다. 캡핑 된 용기를 냉각 한 다음 재결정한다. 이어서, 결정을 여과하고 보관을 위해 분쇄한다 (degroof, S.F.).
물리 화학적 특성
초산 나트륨은 식초 냄새가 나는 백색 흡습성 유리입니다..

무수 형태의 화합물의 경우, 분자량은 82.03 g / mol이고 밀도는 1.5 g / ml이다. 그것의 녹는 점은 섭씨 324도이고 비등점은 881.4도이다..
삼수 화 된 형태에서, 이는 136.03 g / mol의 분자량 및 1.45 g / ml의 밀도를 갖는다. 녹는 점과 끓는 점은 각각 섭씨 58도와 122도까지 급격히 감소합니다..
나트륨 아세테이트는 물에 매우 잘 녹습니다. 수화물의 용해도는 20 개도 섭씨에서 물 100 ㎖의 아세트산 나트륨 46.5 g이며, 그 무수물에 물 100ml 2,017 바이오 내용 (국립 센터 당 123g을 용해시킬 ).
두 형태 모두 아세톤, 메탄올, 히드라진에 용해되며 삼수화물 형태는 에탄올에 용해된다. 나트륨 아세테이트는 단사 결정 구조를 가지고있다 (Royal Society of Chemistry, 2015).
아세트산 나트륨은 아세트산 결합체 염기이므로 pH를 조절하기 위해 아세트산 / 초산 나트륨 용액을 사용하여 완충 용액을 만들 수 있습니다.
물에있는 아세트산 나트륨 용액은 약 알칼리성이다. 열이 섭씨 324도보다 높으면이 염이 분해되어 아세트산 흄이 생성됩니다.
반응성 및 위험성
Sodium acetate는 안정한 화합물로 분류되며 산화제와는 양립 할 수 없다. 가열하면 아세트산 증기와 CO의 방출이 일어날 수있다.2. 이 화합물은 CO 및 CO를 방출하는 고온에서 가연성 일 수 있습니다.2.
아세트산 나트륨의 안전성은 쥐와 생쥐의 동물 모델에서 광범위하게 연구되어 왔습니다. 구강 투여시, 쥐 집단의 절반을 죽이는 치사량은 랫트 체중 kg 당 초산 나트륨 3530mg입니다..
섭취하는 대신 흡입하면, 쥐 인구의 절반을 죽이기 위해 필요한 용량은 30g / m3 / 시간보다 훨씬 높습니다.
생쥐에서 체중 3200 mg / kg의 피하 또는 피하 주사는 쥐의 나트륨 아세테이트 섭취와 비슷한 생쥐 집단의 절반을 죽일 것이다.
그러나 쥐에게 구두로 투여하면 쥐보다 훨씬 더 견딜 수 있습니다. 6891 mg / kg 체중의 쥐 집단 절반의 치사량.
인체에서 아세트산 나트륨 흡입은 기침이나 인후통을 일으킬 수 있지만 피부 나 눈의 직접적인 접촉은 발적과 자극을 유발할 수 있습니다. 그러나 일반적으로 사람의 독성은 미미합니다 (WASSERMAN, 2015).
복통, 메스꺼움, 구토로 소화관에 자극을 줄 수 있으며 비뇨기 계통에 영향을 줄 수 있습니다. 이 화합물을 흡입하면 호흡기가 자극을받을 수 있습니다. 증상으로는 기침, 인후통, 숨가쁨 및 가슴 통증이 있습니다..
눈과의 접촉시 콘택트 렌즈를 검사하고 제거해야합니다. 눈을 즉시 적어도 15 분 동안 물로 충분히 씻어 내야합니다. 차가운 물을 사용할 수 있습니다. 자극이 생기면 치료를 받아야한다..
피부와 접촉 할 경우 비누와 물로 씻어야합니다. 차가운 물을 사용할 수 있습니다. 자극받은 피부는 피부 연화제로 덮여 있습니다. 눈 접촉과 마찬가지로, 자극이 발생하면 의사의 진료를 받아야합니다..
그것이 흡입되면, 희생자는 시원한 장소로 이동해야합니다. 호흡하지 않으면 인공 호흡을 실시해야합니다. 호흡이 어려우면 산소를 공급해야합니다. 다시 한번, 즉시 의학적 치료를받을 필요가 있습니다..
섭취의 경우 의사가 명시하지 않는 한 구토를 유발해서는 안됩니다. 의식이없는 사람에게 입으로 아무것도주지 마라..
셔츠 칼라, 넥타이 또는 벨트와 같은 느슨한 의류는 느슨해 져야합니다. 증상이 나타나면 치료를 받아야합니다 (물질 안전 보건 자료 (Material Safety Data Sheet), 무수 아세트산 나트륨 (Sodium acetate anhydrous), 2013).
취급 및 저장
-화합물은 열 및 발화원으로부터 멀리 보관해야합니다
-빈 용기는 화재 위험이 있으며 추출기 후드 아래에서 잔류 물을 증발시킨다.
-스파크를 피하기 위해 전기 장비는 반드시 접지되어야합니다.
-삼키거나 먼지를들이 마시지 마십시오.
-적절한 보호 복을 착용해야합니다.
-환기가 잘되지 않는 경우 적절한 호흡 장비를 착용해야합니다
-섭취 한 경우에는 즉시 의사에게 가서 용기 나 라벨을 보여야합니다.
-시약은 산화제 및 산과 같은 양립 할 수없는 물질로부터 멀리해야합니다.
-용기를 시원하고 통풍이 잘되는 곳에 보관하는 것 외에도 용기를 단단히 닫아 두십시오..
용도 및 용도
나트륨 아세테이트는 매우 다양한 산업 분야에서 사용됩니다. 섬유 산업에서 나트륨 아세테이트는 아닐린 염료를 사용하면서 황산 폐 스트림과 포토 레지스트를 중성화합니다. 이것은 완성 된 직물의 품질을 향상시킵니다..
사진에서 아세트산 나트륨은 현상액의 일부이며 포토 레지스트로 사용됩니다. 일반적으로 물 침투에 대해 콘크리트를 밀봉하기 위해 사용되는 다른 에폭시보다 환경 친화적 저렴하면서 아세트산 나트륨, 밀봉 제로서 작용하여 콘크리트에서 물에 의한 손상을 완화하기 위해 이용된다.
또한 크롬 유제 처리시 산 세척제이며 합성 고무 생산시 클로로프렌의 가황을 방지합니다. 일회용면 패드 용면 가공에서 나트륨 아세테이트는 정전기 축적을 제거하는 데 사용됩니다.
음식에 첨가 된 초산 나트륨은 방부제 및 향료로 작용합니다. 특히, 아세트산 나트륨을 함유 한 감자 칩은 독특한 "소금 및 식초"맛을 지니고 있습니다.
나트륨 아세테이트는 또한 가열 패드, 온열 장치 및 뜨거운 얼음에도 사용됩니다. 삼수화물의 아세트산 나트륨 결정을 58.4 ℃에서 용융시키고 결정화 수에 용해시킨다.
융점을 초과하여 가열되고이어서 냉각되도록되면, 수용액은 과포화된다. 이 용액은 결정을 형성하지 않고 실온으로 냉각시킬 수 있습니다..
가열 패드에 금속 디스크를 눌러서 핵 형성 센터가 형성되어 용액이 다시 고체 아세트산 나트륨 3 수화물로 결정화되게합니다. 결정화의 결합 형성 과정은 발열 반응이다. 융해 잠열은 약 264-289 kJ / kg이다..
이러한 것들에 의존 불가역 화학 반응과 같은 발열 팩의 일부 유형과 달리, 아세트산 나트륨의 열 팩은 결정이 완전히 용해 될 때까지 몇 분 동안 끓는 물에서 패키지를 침지시킴으로써 쉽게 재사용 될 수있다 그 팩은 실온에 도달 할 때까지 천천히 냉각된다..
완충제로서 아세트산 나트륨 및 아세트산 법 모두 반응 생화학 연구 및 석유 산업 및 화장품 산업에서 비교적 일정한 pH가 유용한 특성을 유지할.
소듐 아세테이트는 작은 핵산의 침전에 사용될 수 있습니다. 이 침전은 flashPAGE의 분획 화 후 더 낮은 기능의 완충액과 같은 희석 된 용액으로부터 작은 핵산을 농축하는데 사용될 수있다.
fracionador의 FlashPage 핵산 미만 2 .mu.g을로드 할 때, 나트륨 아세테이트 / 에탄올로 침전 실행 버퍼로부터 핵산의 최대 회복, 선형 아미드 또는 글리코겐으로 캐리어 하룻밤 권장 느린.
샘플을 DNA 칩 (핵산 소형 S.F.의 아세트산 나트륨 침전)의 해석에 사용하는 것은 캐리어로서 글리코겐을 사용하는 것이 좋다.
의약 분야에서 나트륨 아세테이트 솔루션은 높은 산도 및 / 또는 낮은 나트륨 수준의 환자를 치료합니다.
나트륨은 세포 외액의 주요 양이온입니다. 그것은 약 140mEq / 리터의 정상 혈장 농도에서 총 양이온의 90 % 이상을 차지합니다. 나트륨 이온은 체수 및 그 분포를 제어하는 데 중요한 역할을합니다 (Sodium Acetate, 2010).
아세테이트는 수소 이온 수용체이다. 또한 간에서 대사 전환을위한 중탄산염 (HCO3)의 대체 소스 역할을합니다. 이 전환은 심한 간 질환이있는 경우에도 쉽게 진행되는 것으로 나타났습니다.
물에 희석 된 아세트산 나트륨의 주입은 전해질 보충액으로서 정맥 내 투여된다. 각 20ml에는 나트륨 (Na +)과 아세테이트 (HCO) 40mEq를 제공하는 나트륨 아세테이트 3.28g이 포함되어 있습니다.3-). 이 용액에는 세균 증류 장치, 항균제 또는 완충액이 포함되어 있지 않습니다. 그것은 pH 조절을위한 아세트산 (pH 6.5 (6.0-7.0))을 포함 할 수 있습니다. 오스 몰 농도는 4 mOsmol / ml (calc)이고,.
용액 (2,009 나트륨 아세테이트) 대량 정맥 내 주입 액 외에 나트륨 이온 (NA +)을 제공하기 위해 염화나트륨 대안으로 의도.
나트륨 보존 거기 부종있는 나트륨 이온을 포함하는 솔루션은 특히 울혈 성 심부전, 급성 신부전 환자의 경우 임상 상태에주의하여 사용되어야한다.
신장 기능이 손상된 환자의 경우 나트륨 이온을 함유 한 용액을 투여하면 나트륨이 유지 될 수 있습니다. 아세테이트 이온을 함유 한 용액은 신진 대사 또는 호흡 성 알칼리증 환자에게 큰주의를 기울여 사용해야합니다..
아세트산 심한 간 기능 부전 등의 증가 된 수준 또는이 이온의 손상 활용도가 이러한 조건에 세심한주의 투여되어야.
참고 문헌
- (S.F.). 가정용 성분에서 아세트산 나트륨을 만드는 방법. Recuperado de instructables : instructables.com.
- 물질 안전 보건 자료 무수 초산 나트륨. (2013 년 5 월 21 일). sciencelab에서 가져온 : sciencelab.com.
- 생명 공학 정보 센터. (2017 년 3 월 4 일). PubChem 복합 데이터베이스; CID = 517045 PubChem에서 검색 함.
- 화학 왕립 학회. (2015). 나트륨 아세테이트. chemspider.com에서 가져온.
- 과학자, D. N.-c. (2016, 8 월 12 일). "HOT ICE"- 놀라운 실험. youtube.com에서 가져옴.
- 나트륨 아세테이트. (2009, 5 월 19 일). rxlist에서 가져온.
- 나트륨 아세테이트. (2010, 4 월). drugs.com에서 회복.
- 나트륨 아세테이트 수식. (2005-2017). softschools.com에서 회복.
- 작은 핵산의 아세트산 나트륨 침전. (S.F.). 열 감지기에서 회수.
- WASSERMAN, R. (2015, August 16). 나트륨 아세테이트 염은 무엇입니까? livestrong에서 가져온 것 : livestrong.com.


