에틸 아세테이트 구조, 특성, 합성, 사용 및 위험
그 에틸 아세테이트 또는 에틸에 타노 에이트 (IUPAC 명칭)은 화학식이 CH 인 유기 화합물이다3COOC2H5. 그것은 알코올 성분이 에탄올로부터 유래되는 반면, 그의 카르 복실 산 성분은 아세트산으로부터 유래되는 에스테르로 구성된다.
그것은 온도와 압력의 정상적인 조건에서 액체이며 과일에 즐거운 향기를 선사합니다. 이 속성은 에스터가 기대하는 것과 완벽하게 조화를 이룹니다. 실제로 에틸 아세테이트의 화학적 성질이다. 이런 이유로 그것은 식품 및 알콜 음료에서 사용을 찾습니다.
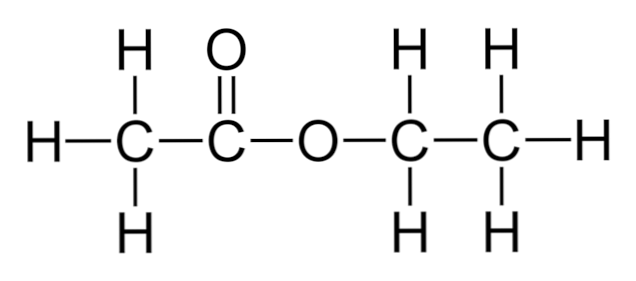
상부 이미지에는 에틸 아세테이트의 구조 골격이 표시되어있다. 왼쪽에는 카르 복실 산 성분이, 오른쪽에는 알코올 성분이 있습니다. 구조적인 관점에서 볼 때,이 화합물은 식초와 알코올 사이의 잡종처럼 행동 할 것으로 기대할 수 있습니다. 그러나, 그것은 그것의 자신의 속성을 나타낸다..
이것은 에스테르라고 불리는 그런 잡종이 다른 것으로서 두드러지는 곳입니다. 에틸 아세테이트는 산으로 반응 할 수 없으며 OH 그룹이없는 상태에서도 탈수 할 수 없습니다. 대신, 그것은 수산화 나트륨, NaOH와 같은 강염기의 존재 하에서 염기성 가수 분해를 거친다..
이 가수 분해 반응은 화학 동역학 실험을 위해 실험실을 가르치는 데 사용됩니다. 또한 반응은 2 차적이다. 가수 분해가 일어날 때, 실제적으로 에틸에 타노 에이트는 그것의 처음 분대에 돌려 보낸다 : 산 (NaOH에 의하여 deprotonated) 및 알콜.
구조 골격에서 수소 원자가 산소 원자보다 우세하다는 것이 관찰됩니다. 이것은 지방과 같은 비극성 종과 상호 작용하는 능력에 영향을 미친다. 또한 수지, 염료 및 일반 유기 고체와 같은 화합물을 용해시키는 데에도 사용됩니다.
유쾌한 향기에도 불구하고,이 액체에 장기간 노출되면 몸에 거의 모든 화학 물질과 같은 부정적인 영향을줍니다.
색인
- 1 에틸 아세테이트의 구조
- 1.1 수소 공여체 원자의 부재
- 2 물리 화학적 특성
- 2.1 이름
- 2.2 분자식
- 2.3 분자량
- 2.4 물리적 설명
- 2.5 색
- 2.6 냄새
- 2.7 맛
- 2.8 악취 문턱
- 2.9 끓는점
- 2.10 융점
- 2.11 물 용해도
- 2.12 유기 용매에서의 용해도
- 2.13 밀도
- 2.14 증기 밀도
- 2.15 안정성
- 2.16 증기압
- 2.17 점도
- 2.18 연소열
- 2.19 기화열
- 2.20 표면 장력
- 2.21 굴절률
- 2.22 보관 온도
- 2.23 pKa
- 3 요약
- 3.1 피셔의 반응
- 3.2 티쉬 첸코 반응
- 3.3 다른 방법들
- 4 용도
- 4.1 용제
- 4.2 인공 향료
- 4.3 애널리틱스
- 4.4 유기 합성
- 4.5 크로마토 그래피
- 4.6 곤충학
- 5 가지 위험
- 6 참고 문헌
에틸 아세테이트의 구조
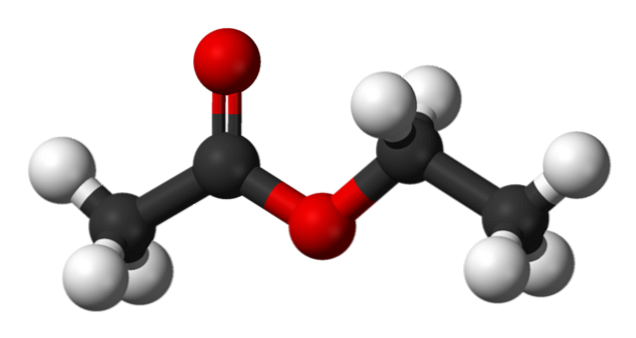
상부 이미지에서 에틸 아세테이트의 구조는 구체와 막대의 모델로 표시됩니다. 이 모델에서는 빨간 구체가있는 산소 원자가 강조 표시됩니다. 왼쪽은 산으로부터 유도 된 분획이고, 오른쪽은 알코올 (알콕시 기, -OR)로부터 유도 된 분획이며,.
카르 보닐 기는 C = O 결합 (이중 막대)에 의해 평가된다. 이 그룹과 인접한 산소 주변의 구조는 두 산소 사이의 공진에 의한 하중의 역전이 있기 때문에 평평하다. 이는 α 수소의 상대적으로 낮은 산성도를 설명하는 사실이다 (-CH 그룹3, C = O에 연결된).
분자는 두 개의 결합을 회전시킴으로써 다른 분자와 어떻게 상호 작용하는지 직접적으로 선호합니다. 두 개의 산소 원자의 존재와 구조의 비대칭은 영구 쌍극자 모멘트를 준다. 이것은 차례로 쌍극자 - 쌍극자 상호 작용에 대한 책임이있다..
예를 들어, 전자 밀도는 2 개의 산소 원자 근처에서 더 크며, 그룹 -CH3, 점진적으로 OCH 그룹에2CH3.
이러한 상호 작용으로 인해 에틸 아세테이트 분자는 정상 조건에서 액체를 형성하며, 이는 상당히 높은 비점 (77 ℃).
수소 결합의 기증자 원자가 부재하다.
구조를 면밀히 살펴보면 수소 교량을 기증 할 수있는 원자가 없음을 알 수 있습니다. 그러나 산소 원자는 그러한 수용체이며 에틸 아세테이트는 물에 매우 잘 녹고 극성 화합물과 수소 결합 공여체 (설탕과 같은)와 상당한 정도로 상호 작용하며,.
또한, 이것은 에탄올로 탁월하게 상호 작용할 수있게합니다; 알코올성 음료에서 그 존재가 놀라운 것이 아닌 이유입니다..
다른 한편, 그것의 알콕시 그룹은 클로로 폼, CH3Cl.
물리 화학적 특성
이름
-에틸 아세테이트
-에틸에 타노 에이트
-아세트산 에스테르
-아세 톡시 에탄
분자식
C4H8O2 또는 CH3COOC2H5
분자량
88,106 g / 몰.
물리적 설명
무색 투명한 액체.
색상
무색의 액체.
냄새
파인애플 냄새와 비슷한 에테르의 특징.
맛
묽게 할 때 기분이 좋으며 맥주에 과일 맛을 더합니다.
악취 문턱
3.9 ppm. 0.0196 mg / m3 (낮은 냄새); 665 mg / m3 (높은 냄새).
7 - 50 ppm (평균 = 8 ppm)에서 감지 할 수있는 냄새.
끓는점
171 ° F ~ 760 mmHg (77.1 ° C).
융점
-118.5ºF (-83.8ºC).
물에 대한 용해도
80g / L.
유기 용제의 용해도
에탄올과 에틸 에테르와 섞일 것. 아세톤 및 벤젠에 매우 잘 용해됩니다. 클로로포름, 고정 및 휘발성 오일 및 산화 및 염소화 용제와도 혼 화성 있음.
밀도
0.9003 g / cm3.
증기 밀도
3.04 (공기비 : 1).
안정성
그것은 수분과 함께 천천히 분해된다. 여러 가지 플라스틱 및 강한 산화제와는 호환되지 않습니다. 물과의 혼합물은 폭발성 일 수 있습니다..
증기 압력
25 ° C에서 93.2 mmHg
점도
25 ºC에서 0.423 mPoise.
연소열
2,238.1kJ / mol.
기화열
25 ºC에서 35.60 kJ / mol.
표면 장력
20 ºC에서 24 다인 / cm.
굴절률
20 ° C / D에서 1,373.
보관 온도
2 - 8 ºC.
pKa
25 - 24도에서 16 - 18.
합성
피셔의 반응
에틸 아세테이트는 피셔 (Fisher) 반응에 의해 산업적으로 합성되며, 에탄올은 아세트산으로 에스테르 화된다. 반응은 실온에서 수행된다.
CH3CH2OH + CH3COOH <=> CH3쿡2CH3 + H2O
반응은 산 촉매에 의해 촉진된다. 평형은 물의 제거를 통해 에틸 아세테이트 생산을 향한 오른쪽으로 이동합니다. 매스 액션 법에 따라.
Tishchenko의 반응
에틸 아세테이트는 또한 Tishchenko 반응을 사용하여 공업 적으로 제조되며, 2 당량의 아세트 알데히드를 촉매로서 알콕시 드.
2 CH3CHO => CH3쿡2CH3
다른 방법들
-에틸 아세테이트는 175 ℃ 및 50 기압의 온도에서 수행되는 반응에서 부탄의 아세트산으로의 산화에서 부산물로서 합성된다. 코발트 및 크롬 이온은 촉매로 사용됩니다..
-에틸 아세테이트는 폴리 비닐 아세테이트의 폴리 비닐 알콜에 대한 에탄올 분해의 부산물이다..
-에틸 아세테이트는 또한 에탄올의 탈수 소화에 의해 산업에서 생성되며,이 반응은 승온에서 구리의 사용에 의해 촉매 화되지만 250 ℃ 미만이다..
용도
용제
에틸 아세테이트는 용매 및 희석제로 사용되며 회로 기판의 청소에 사용됩니다. 그것은 수정 된 홉 추출물의 제조 및 커피와 찻잎의 카페인 제거에서 용매로 사용됩니다. 과일과 채소를 표시하는 데 사용되는 잉크에 사용됩니다..
에틸 아세테이트는 섬유 산업에서 세정제로 사용됩니다. 이것은 당의 분리에 사용되는 온도계 보정에 사용됩니다. 도료 업계에서는 사용 된 재료의 용제 및 희석제로 사용됩니다.
인공 향료
그것은 과일 풍미의 정교화에서 사용된다; 예 : 바나나, 배, 복숭아, 파인애플, 포도 향기 등.
분석
그것은 비스무트, 붕소, 금, 몰리브덴 및 백금뿐만 아니라 탈륨 용매의 측정에 사용됩니다. 에틸 아세테이트는 인, 코발트, 텅스텐 및 비소와 같이 수용액에 존재하는 많은 화합물과 원소를 추출하는 능력이 있습니다..
유기 합성
에틸 아세테이트는 포토 레지스트 제형에 사용되는 수지의 점도 감소 제로서 업계에서 사용됩니다. 아세트 아미드, 아세틸 아세테이트 및 메틸 헵 타논의 생산에 사용됩니다..
크로마토 그래피
실험실에서 에틸 아세테이트는 칼럼 크로마토 그래피의 이동상 및 추출 용매로 사용됩니다. 에틸 아세테이트의 비점이 비교적 낮 으면 증발되기 쉽기 때문에 용제를 용매에 농축시킬 수있다.
곤충학
에틸 아세테이트는 곤충에서 추출한 곤충을 질식시켜 곤충을 수집하고 연구 할 수있게합니다. 에틸 아세테이트의 증기는 곤충을 파괴하지 않고 곤충을 죽이고 그것의 경화를 방지하여 수집을위한 조립을 용이하게한다..
위험
-LD50 의 에틸 아세테이트는 낮은 독성을 나타낸다. 그러나 피부, 눈, 피부, 코와 목을 자극 할 수 있습니다..
-높은 수준에 노출되면 현기증과 졸도를 유발할 수 있습니다. 또한 장기 노출은 간과 신장에 영향을 줄 수 있습니다..
-20,000 - 43,000 ppm 농도의 에틸 아세테이트를 흡입하면 폐부종과 출혈을 유발할 수 있습니다.
-작업장 노출 한도는 8 시간 작업 교대 중에 평균 400ppm의 대기 중 OSHA에 의해 설정되었습니다.
참고 문헌
- Steven A. Hardinger. (2017). 유기 화학 용어 설명 : 에틸 아세테이트 (EtOAc). 원본 주소 'chem.ucla.edu'
- Graham Solomons T.W., Craig B. Fryhle. (2011). 유기 화학. 아민 (10일 판.). 와일리 플러스.
- Morrison, R.T. and Boyd, R.N. (1990). 유기 화학 (5타 판). 편집 Addison-Wesley Iberoamericana.
- 위키 백과. (2019). 에틸 아세테이트. 원본 주소 'en.wikipedia.org'
- 코튼 S. (s.f.). 에틸 아세테이트. 원본 주소 'chm.bris.ac.uk'
- PubChem. (2019). 에틸 아세테이트. 원본 주소 'pubchem.ncbi.nlm.nih.gov'
- Newseed Chemical. (2018). 에틸 아세테이트의 응용 및 사용. 원본 주소 찾기 : foodsweeteners.com
- 뉴저지 보건부 고령 서비스. (2002). 에틸 아세테이트. [PDF] 원본 주소 'nj.gov'


