수산화 칼슘 수식, 특성, 반응성 및 용도
그 수산화칼슘, 수화 석회 또는 소석회로도 알려져 있으며, 화학식 Ca (OH)2.
수산화칼슘은 모든 금속 수산화물과 마찬가지로 수산화 마그네슘 (Mg (OH))과 동일한 고분자 구조를 취합니다.2) brucita라고도합니다..
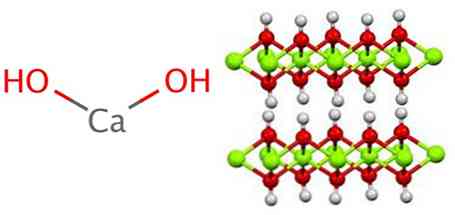
이 구조에서 수소 교량이 형성되어 있음을 알 수 있습니다. 수산화칼슘은 다음 반응에 따라 석회 또는 생석회라고도 알려진 산화 칼슘을 물과 반응시켜 공업 적으로 합성됩니다 :
CaOH + H2O → Ca (OH)2
또한 실험실에서 수성 염화칼슘과 수산화 나트륨 사이의 반응으로 제조됩니다.
수산화칼슘은 자연적으로 발생하지만 일부 화산 및 변성암에서 발견되는 포틀랜드 (portlandite)와 같은 미네랄 형태에서는 거의 발생하지 않습니다. (수산화칼슘 공식 - 수산화칼슘 용도, 재산, 구조 및 공식 2005-2017 년).
이 화합물은 시멘트, 용제 및 산업용 세정제 (건축 제품과 같은), 바닥 제거제, 벽돌 세정제, 시멘트 농축 제품 및 기타 여러 제품에서 일반적으로 사용 가능합니다..
수용액은 일반적으로 석회 (limewater) 라 불린다. 석회수는 수산화칼슘을 순수한 물에 넣고 과량의 Ca (OH)2 해산되지 않은.
과량의 수산화칼슘이 석회수에 첨가 될 때 수산화칼슘 입자의 현탁액이 얻어지며 유백색의 외관을 갖게된다.이 경우 일반 이름은 라임 밀크이다. 석회유 또는 석회 (석회수)의 포화 용액은 pH가 12.3이며 기본 성질을 띤다..
수산화칼슘의 물리적 및 화학적 성질
수산화칼슘은 냄새가없는 흰색 또는 무색의 분말입니다. 수용액 (포화 용액)에서 용해되지 않은 수산화칼슘의 상징액으로 인해 유백색을 띄게됩니다.
불포화 용액은 보통 맑고 무색의 용액으로 약간의 흙 냄새와 칼슘 수산화물의 알칼리성 맛이 있습니다. 이 화합물의 외관은 그림 3 (Royal Society of Chemistry, 2015).

수산화칼슘은 고체 상태에서 74.093 g / mol의 분자량 및 2.211 g / cm3의 밀도를 갖는다. 그것은 섭씨 580 도의 녹는 점이 있습니다. 그것은 물에 잘 녹지 않으며, 0 ℃에서 1.89g, 20 ℃에서 1.73g, 100 ℃에서 0.66g을 용해시킬 수있다.
그것은 글리세롤과 산 용액에 용해됩니다. 알코올에 녹지 않는다 (National Center for Biotechnology Information, S.F.).
수산화칼슘은 부분적으로 물에 용해되어 온화한 기반 인 석회질이라고 불리는 용액을 생성합니다. 석회수 또는 Ca (OH)2 (aq) 그것은 산과 반응하여 염을 형성하고 알루미늄과 같은 일부 금속을 공격 할 수 있습니다. 석회수는 이산화탄소와 쉽게 반응하여 탄산염이라고하는 유용한 공정 인 탄산 칼슘을 형성합니다.
Ca (OH)2 + 콜로라도 주2 → CaCO3 + H2O
니트로 파라핀, 니트로 메탄, 니트로 프로판 등은 수산화칼슘과 같은 무기 염기와 염을 형성한다. 이 건조한 소금은 폭발적입니다. 이 화합물은 화학적으로 수산화 나트륨 (NaOH) 또는 산화 나트륨 (Na2O). 이것들은 산을 발열 반응시켜 염과 물을 형성한다..
이러한 물질을 물과 혼합하면 염기가 용해되거나 희석되기 때문에 위험하지 않은 양의 열이 발생할 수 있습니다. 염기는 특정 금속 (예 : 알루미늄 및 아연)과 반응하여 금속 산화물 또는 수산화물을 형성하고 수소 가스를 발생시킵니다..
염기는 중합 가능한 유기 화합물, 특히 에폭 사이드에서 중합 반응을 개시 할 수있다. 가연성 및 / 또는 독성 가스는 암모늄염, 질화물, 할로겐화 유기물, 다양한 금속, 과산화물 및 하이드 로퍼 옥사이드로 생성 될 수 있습니다. 이러한 유형의 화합물은 종종 촉매 역할을합니다 (Chemical Datasheet CALCIUM HYDROXIDE, S.F.).
반응성 및 위험성

수산화칼슘은 강산과 양립 할 수 없지만 안정한 화합물입니다. 그것은 자극성 화합물로 분류되며, 우리는 다음과 같은 위험성을 강조 할 수 있습니다 :
눈에 부식성이 있으며 (각막 손상이나 실명을 유발할 수 있음) 피부 (염증과 수포가 생성됨).
분진을 흡입하면 위장관이나 호흡기에서 자극을 유발할 수 있으며 이는 연소, 재채기 및 기침을 특징으로합니다. 심한 과다 노출은 폐 손상, 질식, 의식 불명 또는 사망을 유발할 수 있습니다. 눈의 염증은 발적, 자극 및 가려움으로 특징 지어 짐 (물질 안전 보건 자료, Calcium hydroxide, 2013).
낮은 분진의 눈에 반복적으로 노출되면 피부에 자극과 국부적 인 피부 파괴 또는 피부염을 유발할 수 있습니다. 반복적 인 분진 흡입은 다양한 수준의 호흡기 자극이나 폐 손상을 일으킬 수 있음..
이 화학 물질이 눈에 들어갔을 경우 다량의 물로 즉시 씻어 내고 때때로 아래 눈꺼풀과 위쪽 눈꺼풀을 들어야합니다. 즉시 의학적 치료를 받아야합니다. 이 화학 물질로 작업 할 때 콘택트 렌즈를 사용하면 안됩니다..
이 화학 물질이 피부에 접촉되면 비누와 물로 오염 된 피부를 즉시 씻어 내야합니다. 이 화학 물질이 옷에 침투하면 즉시 옷을 벗고 물로 피부를 헹구십시오. 세척 후에도 자극이 지속되면 의료 조치를 취하십시오..
다량의이 화학 물질을 흡입하면 노출 된 사람을 즉시 신선한 공기로 이동시켜야합니다. 호흡이 멈춘 경우, 구강 대 구강 인공 호흡을 실시하고 피해자를 따뜻하게하고 쉬게하십시오. 가능한 한 빨리 의료 조치를 취하십시오..
섭취 한 경우 즉시 의학적 조언을 구하고 가능한 경우 용기 또는 라벨을 보일 것. (Calcium hydroxide poisoning, 2017).
취급 및 저장
- 화합물은 건조한 용기에 보관해야합니다.
- 먼지를 섭취하거나 호흡하지 마십시오..
- 물을이 제품에 절대로 첨가해서는 안됩니다..
- 환기가 잘되지 않는 경우 적절한 호흡 장비를 가져 오십시오.
- 피부 및 눈과의 접촉을 피하십시오..
- 산과의 양립 불가능성에 가까이하지 말 것..
- 용기를 단단히 닫아 두십시오..
- 시원하고 통풍이 잘되는 곳에 용기를 보관하십시오. 섭씨 25도 이상에서 보관하지 마십시오..
용도 및 용도

수산화칼슘은 대규모로 생산되며 쉽게 다룰 수 있으며 일반적으로 값이 싸다. 그러므로 많은 주목할만한 용도와 용도가있다..
수산화칼슘의 중요한 용도는 물 및 폐수 처리에서 응집제와 같습니다. 물에서 더 작은 입자를 제거하는 데 도움이되는 가벼운 충전 된 고체를 형성하여 더 가벼운 제품을 만듭니다..
이 응용 프로그램은 수산화칼슘의 낮은 비용과 낮은 독성으로 가능합니다. 그것은 또한 담수의 pH를 올리기위한 처리에 사용됩니다. 목적은 기본 물이 산성 인 곳에서 파이프가 부식되지 않는다는 것입니다.
또 다른 훌륭한 응용 분야는 제지 산업에 있으며 수산화 나트륨 생산에 사용됩니다. 이 전환은 펄프의 추출에 사용되는 공지 된 크래프트 공정의 성분이다.
이산화탄소 스크러버와 같은 생명 유지 시스템, 특히 부식성이 강한 수산화 리튬이 너무 위험하다고 생각되는 폐회로 다이빙 용 재 호흡기.
그것은 소위 석회 모르타르와 함께 표백 및 석고에서 성분으로 사용됩니다. 도로 건설에서 수산화칼슘은 토양의 품질을 향상시키는 역할을합니다..
국립 보건원 (National Institutes of Health)에 따르면, 수산화칼슘은 항균제로 치과 치료에 일반적으로 사용되며 첨단 장벽 (pical barrier)으로 알려진 보호 층을 형성하기위한 선택의 실체입니다..
Apical barrier는 치열 교정 수술이 특히 어려울 수있는 상황에서 pulpal 괴사를 피하는 수단으로 일반적으로 사용됩니다. 이는 일반적으로 미성숙 영구 치아의 결과입니다.
수산화칼슘은 감염이 이미 존재하는 치아를 소독하는 데 도움이되므로 근관 치료를 준비 할 때 통증과 염증을 줄이기위한 단기 치료로 사용할 수 있습니다 (Gottfried Schmalz, 2009).
그것은 대기 CO2를 줄이고 온실 효과를 완화시키기 때문에 바닷물의 첨가제 역할을합니다..
금속 생산시 석회는 폐가스 흐름에 주입되어 불소 및 염화물과 같은 산을 중화시켜 대기로 방출합니다.
수산화칼슘은 일부 모발 이완 제품에서 활성 알칼리 성분으로 사용됩니다.
Cornell 재료 연구 센터에 따르면 수산화칼슘은 자연스러운 곱슬 머리에 고농도로 존재하는 아미노산 인 시스테인을 연결하는 이황화 결합을 끊기 때문에 곱슬 머리를 곧게 만듭니다. 이러한 결합을 끊고 수산화칼슘으로 밀봉하면 영구적으로 처리 된 모발의 물리적 구조가 바뀝니다.
보르도 혼합물에서 수산화칼슘은 용액을 중화시키고 오래 지속되는 살균제를 형성합니다.
그것은 석유 첨가제 (salicylates, sulphics, 페놀)의 제조를위한 석유 정제 산업, 다양한 브랜드의 고체 오일 제조를위한 석유 화학 산업 및 화학 산업에서 칼슘 스테아 레이트 제조를 위해 사용됩니다 . 그것은 일반적으로 이산화탄소 및 가스 흡수 검사에 사용됩니다.
수산화칼슘은 브레이크 패드의 제조, 페인트 및 장식용 건조 혼합물의 제조 및 살충제 혼합물의 제조에 사용됩니다.
암초 수족관의 산호 양식을위한 칼슘 보충제 및 pH / 탄산염 완충액으로도 사용됩니다..
"대체"천연 살충제인데, 대부분의 크롤링 곤충은 진드기, 벼룩, 딱정벌레 및 애벌레를 포함한 그것과 접촉하여 사망합니다 (Russiver, 2015).
수산화칼슘은 동물의 가죽에서 모발을 분리하고 가죽의 제조를 위해 효과적인 솔루션입니다.
수산화칼슘과 따뜻한 물의 혼합물은 신선한 가죽을 4 일간 담가 두어 자주 흔들어야하는 욕조를 만듭니다. 이 과정은 일반적으로 손으로 제거 할 수있을 정도까지 모발과 피부를 풀어줍니다..
독성이 낮고 기본 성질이 부드럽기 때문에 소석회는 식품 업계에서 널리 사용됩니다.
- 설탕 산업에서 사탕 수수 또는 사탕무의 원료 주스를 명확히하기 위해 주류 및 청량 음료, 절임 및 기타 식품에 대한 공정 수.
- 옥수수 토틸라를 만드십시오 (옥수수가 함께 오도록 도와주세요). 석회로 조리 한 옥수수는 nixtamal로 전환되어 니아신의 생체 이용률을 현저히 증가 시키며 맛이 좋고 소화하기 쉽습니다..
- 식품 및 의약품 용 소금 제조시 칼슘 및 마그네슘 카보네이트 염수를 세척하십시오.
- 오렌지 주스, 유아용 조제와 같은 과일 음료를 강화하십시오 (BAUM, 2013).
참고 문헌
- BAUM, J. (2013 년 8 월 16 일). 수산화 칼슘 사용. livestrong.com에서 가져온 : livestrong.com.
- 칼슘 수산화물 공식 - 칼슘 수산화물 용도, 특성, 구조 및 공식. (2005-2017). softschools.com에서 가져온.
- 수산화 칼슘 중독. (2017 년 2 월 7 일). medlineplus.gov에서 가져옴.
- 화학 물질 데이터 시트 수산화 칼슘. (S.F.). cameochemicals.noaa.gov에서 검색 함.
- Gottfried Schmalz, D. A. (2009). 치과 재료의 생체 적합성. 베를린 : 스프링 어.
- 물질 안전 보건 자료 Calcium hydroxide. (2013 년 5 월 21 일). sciencelab에서 가져온 : sciencelab.com.
- 생명 공학 정보 센터. (S.F.). PubChem 복합 데이터베이스; CID = 6093208. pubchem.ncbi.nlm.nih.gov에서 가져옴.
- 화학 왕립 학회. (2015). 수산화칼슘. ChemSpider에서 가져온 항목 : chemspider.com.
- Russiver, M. (2015, August 17). 수산화칼슘이란 무엇입니까? quora에서 가져온 것 : quora.com.


