베릴륨 하이드 록 사이드 (Be (OH) 2) 화학 구조, 특성 및 용도
그 수산화 베릴륨 는 수산화물 (OH)과 베릴륨 (Be) 분자의 두 분자로 이루어진 화합물입니다. 그것의 화학 공식은 Be (OH)2 그것은 양서류 인 것을 특징으로한다. 일반적으로 다음과 같은 화학 반응에 따라 베릴륨 모노 옥사이드와 물의 반응에서 얻을 수 있습니다 : BeO + H2O → Be (OH)2
한편,이 양성 물질은 선형 형태의 분자 구조를 갖는다. 그러나, 베릴륨 하이드 록 사이드의 다양한 구조가 얻어 질 수있다 : 알파 및 베타 형태, 광물 및 증기 상, 사용 된 방법에 따른다..
색인
- 1 화학 구조
- 1.1 베릴륨 하이드 록 사이드 알파
- 1.2 Beta 베릴륨 수산화물
- 1.3 광물에서 수산화 베릴륨
- 1.4 베릴륨 하이드 록 사이드의 증기
- 2 속성
- 2.1 외관
- 2.2 열 화학적 성질
- 2.3 용해도
- 2.4 노출로 인한 위험
- 3 용도
- 4 얻기
- 4.1 금속 베릴륨 얻기
- 5 참고
화학 구조
이 화합물은 네 가지 방법으로 찾을 수 있습니다 :
베릴륨 하이드 록 사이드 알파
베릴륨 염 용액에 수산화 나트륨 (NaOH)과 같은 염기성 시약을 첨가함으로써 수산화 베릴륨의 알파 (α) 형태가 얻어진다. 다음은 그 예입니다.
2NaOH (희석 된) + BeCl2 → Be (OH)2↓ + 2NaCl
2NaOH (희석) + BeSO4 → Be (OH)2↓ + Na2그래서4
베릴륨 베타 수산화물
이 알파 생성물의 퇴화는 준 안정 정방 결정 구조를 형성하며, 장시간 동안 베릴륨 히드 록 시드 베타 (베릴륨 하이드 록 사이드 베타 (β)) 라 불리는 마름모 구조로 변형되고,.
이 베타 형태는 또한 융점에 가까운 조건에서의 가수 분해에 의한 베릴륨 나트륨 용액으로부터의 침전물로서 얻어진다.
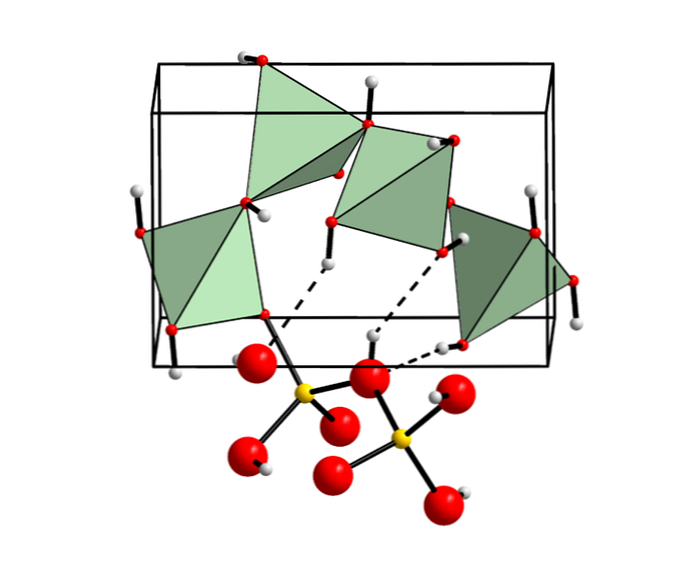
미네랄의 수산화 베릴륨
베릴륨 수산화물은 보통은 아니지만 결정체로 알려져 있습니다 (화학적 조성과 관련하여 이런 식으로 불림).
그것은 화산의 fumaroles에서 Gadolinite (규산염 군의 광물)의 변화에 의해 형성된 화강암 질 페그마타이트에서 일어난다.
이 비교적 새로운 광물은 1964 년에 처음 발견되었으며 현재 미국 텍사스 주와 유타 주에 위치한 화강암 페그마타이트에서만 발견됩니다..
베릴륨 하이드 록 사이드의 증기
1200 ° C (2190 ° C) 이상의 온도에서 수산화 베릴륨은 증기 상에 존재합니다. 이것은 수증기와 베릴륨 산화물 (BeO) 사이의 반응으로부터 얻어진다..
유사하게, 생성 된 증기는 1500 ℃의 온도에서 측정 된 73 Pa의 분압을 갖는다.
등록 정보
베릴륨 하이드 록 사이드는 몰 질량 또는 대략 분자량이 43.0268 g / mol이고 밀도가 1.92 g / cm이다3. 녹는 점은 1000 ℃의 온도에서 분해가 시작됩니다.
광물로서 Be (OH)2 (behoita)는 4의 경도를 가지고 밀도는 1.91 g / cm3 및 1.93 g / cm3.
외관
베릴륨 하이드 록 사이드는 백색 고체이며 알파 형태는 젤라틴과 비정질로 나타난다. 한편,이 화합물의 베타 형태는 잘 정의 된 사방 정계 및 안정한 결정 구조로 구성됩니다.
Be (OH)의 광물의 형태는,2 그것은 망상 결정, 교목 또는 구형 응집체로서 발견 될 수 있기 때문에 다양하다. 마찬가지로, 흰색, 분홍색, 푸른 색, 심지어 무색이며 기름기 많은 유리 광택이 있습니다.
열 화학적 성질
엔탈피 형성 : -902.5 kJ / mol
깁스 에너지 : -815.0 kJ / mol
생성 엔트로피 : 45.5 J / mol
열용량 : 62.1 J / mol
비열 용량 : 1,443 J / K
표준 생성 엔탈피 : -20.98 kJ / g
용해도
수산화 베릴륨은 본질적으로 양쪽 성이므로 양성자를 기증하거나 수용 할 수 있으며 산 - 염기 반응에서 산성 및 염기성 매체를 모두 용해시켜 소금과 물을 생성합니다.
이러한 의미에서, Be (OH)2 물에서의 용해도 곱은 Kps(H2O), 6.92 × 10과 같다.-22 개월.
노출 위험
최대 농도가 0.002 mg / m3 인 베릴륨 수산화물의 법적으로 허용되는 인체 노출 한도 (PEL 또는 OSHA)3 및 0.005 mg / m3 8 시간, 0.0225 mg / m33 최대 30 분.
이러한 제한은 베릴륨이 발암 성 물질 유형 A1 (역학 연구에서 나온 증거의 양을 기반으로 인간의 발암 성 물질)으로 분류된다는 사실에 기인합니다..
용도
베릴륨 하이드 록 사이드를 일부 제품의 가공을위한 원료로 사용하는 것은 매우 제한적이다. 그러나, 다른 화합물의 합성 및 베릴륨 금속의 수득을위한 주된 시약으로 사용되는 화합물이다.
구하기
베릴륨 산화물 (BeO)은 업계에서 가장 많이 사용되는 고순도 베릴륨 화합물입니다. 전기 절연성 및 높은 열 전도성을 갖는 무색 고체로 특징 지어 짐..
이러한 의미에서, 1 차 산업에서 (기술적 품질에서) 합성하는 과정은 다음과 같은 방식으로 수행됩니다 :
- 수산화 베릴륨은 황산 (H2그래서4).
- 반응이 수행 될 때, 용액은 여과되어, 산화물 또는 황산염의 불용성 불순물이 이러한 방식으로 제거된다..
- 여액을 증발시켜 생성물을 농축시키고,이를 냉각시켜 베릴륨 술 페이트의 결정4.
- BeSO4 1100 ℃와 1400 ℃ 사이의 특정 온도에서 소성된다..
최종 제품 (BeO)은 산업용 특수 세라믹 조각 제조에 사용됩니다.
금속 베릴륨 얻기
베릴륨 광물의 추출 및 가공 과정에서 베릴륨 산화물 및 베릴륨 수산화물과 같은 불순물이 생성된다. 후자는 금속 베릴륨을 얻을 때까지 일련의 변환을 거친다..
Be (OH)2 암모늄 비 플루오 라이드의 용액으로 :
Be (OH)2 + 2 (NH4) HF2 → (NH4)2BeF4 + 2 H2O
(NH4)2BeF4 그것은 온도의 상승에 영향을 받아 열분해된다.
(NH4)2BeF4 → 2NH3 + 2HF + BeF2
마지막으로, 마그네슘 (Mg)을 사용하여 1300 ° C에서 베릴륨 플루오 라이드를 환원하면 베릴륨 금속이 생성됩니다.
BeF2 + Mg → Be + MgF2
베릴륨은 금속 합금, 전자 부품 생산, X 선 장치에 사용되는 방사선 스크린 및 창 제조에 사용됩니다..
참고 문헌
- 위키 백과. (s.f.). 수산화 베릴륨. en.wikipedia.org에서 검색
- Holleman, A. F .; Wiberg, E. 및 Wiberg, N. (2001). 수산화 베릴륨. books.google.co.ve에서 가져옴
- Publishing, M.D. (s.f.). Behoite. handbookofmineralogy.org에서 검색 함
- 모든 반응. (s.f.). 수산화 베릴륨 (Be) (OH)2. allreactions.com에서 검색 함
- PubChem. (s.f.). 수산화 베릴륨. pubchem.ncbi.nlm.nih.gov에서 가져옴
- Walsh, K.A. 및 Vidal, E.E. (2009). 베릴륨 화학 및 공정. books.google.co.ve에서 가져옴


