브롬화 수소산 (HBr) 구조, 특성, 형성, 용도
그 브롬화 수소산 브롬화 수소 (hydrogen bromide) 라 불리는 가스의 수용액으로부터 생성 된 무기 화합물이다. 그것의 화학 공식은 HBr이며 다른 방법으로 동일하게 간주 될 수 있습니다 : 분자 수소 또는 물의 할로겐화 수소; 즉, 히드라 지드.
화학 반응식에서 브롬 산이 아니라 가스임을 나타 내기 위해 HBr (ac)로 표기해야합니다. 이 산은 염산, HCl보다 훨씬 더 강력한 것으로 알려져 있습니다. 이것에 대한 설명은 공유 결합의 성질에있다..
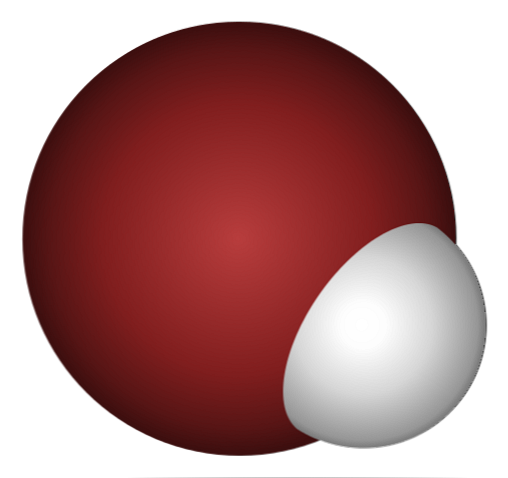
왜 HBr은 산성이며 물에 더 많이 용해됩니까? 공유 결합 H-Br는 H의 1s 오비탈과 Br의 4p의 중첩이 잘 이루어지지 않아 매우 약하기 때문에.
브롬 원자 (갈색)가 수소 원자 (흰색)보다 훨씬 큰 위의 이미지를 자세히 보면 놀라지 않습니다..
결과적으로, 어떠한 교란이라도 H-Br 결합이 파괴되어 H 이온이 방출된다+. 브롬 스틴 산 (Brönsted acid)은 양성자 또는 수소 이온을 전달하기 때문에 브 st스 테드 산 (Brönsted acid)입니다. 이의 강도는 여러 가지 유기 브롬화 화합물 (예 : 1- 브로 모 에탄, CH3CH2Br).
브롬화 수소산은 수 소화물, HI 다음에 특정 고체 시료의 소화를위한 가장 강력하고 유용한 수산화물 중 하나입니다.
색인
- 1 브롬화 수소산의 구조
- 1.1 산성도
- 2 물리 화학적 특성
- 2.1 분자식
- 2.2 분자량
- 2.3 외관
- 2.4 냄새
- 2.5 악취 문턱
- 2.6 밀도
- 2.7 융점
- 2.8 끓는 점
- 2.9 물 용해도
- 2.10 증기 밀도
- 2.11 pKa 신맛
- 2.12 칼로리 용량
- 2.13 표준 몰 엔탈피
- 2.14 표준 몰 엔트로피
- 2.15 인화점
- 3 명칭
- 4 어떻게 형성 되는가??
- 4.1 물에서 수소와 브롬의 혼합
- 4.2 삼 브롬화 인
- 4.3 이산화황 및 브롬
- 5 용도
- 5.1 브롬화물의 제조
- 5.2 알킬 할라이드의 합성
- 5.3 촉매
- 6 참고 문헌
브롬화 수소산의 구조
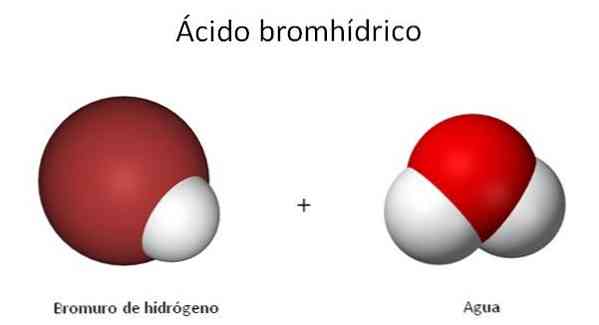
H-Br의 구조는 이미지에 나타나는데, 가스의 특성과 특성이 수용액과 밀접한 관련이 있습니다. 그렇기 때문에 HBr 또는 HBr (ac)와 HBr (HBr)의 두 화합물에 대해 혼란 스러울 때가 있습니다..
HBr (ac)의 구조는 HBr의 구조와 다르다. 왜냐하면 물 분자가이 이원자 분자를 용매 화하기 때문이다. 그것이 충분히 가까울 때, H가 전송된다+ H의 분자에2또는 다음의 화학 반응식에 나타나있는 바와 같이 :
HBr + H2O => Br-- + H3O+
따라서, 브롬 산 (bromobic acid)의 구조는 Br 이온-- 및 H3O+ 정전기와 상호 작용한다. 이제는 H-Br의 공유 결합과는 조금 다릅니다..
그것의 위대한 신맛은 부피가 큰 음이온 Br 때문입니다- 간신히 H와 상호 작용할 수있다.3O+, 그가 H를 옮기는 것을 막을 수 없다.+ 다른 주변 화학 종으로.
산성도
예를 들어, Cl- 와 F- 그들은 H와 공유 결합을 형성하지는 않지만3O+, 그들은 수소 교량과 같은 다른 분자간 힘을 통해 상호 작용할 수있다 (F- 그 (것)들을 받아 들일 수있다). 수소 교량 F--H-OH2+ H의 기부를 "방해"합니다.+.
HF가 불화 수소산 인 이유는 약산 물속에 브롬 산; 왜냐하면, 이온 상호 작용 Br- H3O+ H 이동을 방해하지 마라.+.
그러나 물이 HBr (ac)에 존재하기는하지만, 계정 말미의 행동은 H-Br 분자의 행동과 유사합니다. 즉, H+ 그것은 HBr 또는 Br에서 옮겨진다.-H3O+.
물리 화학적 특성
분자식
HBr.
분자량
80,972 g / mol. 이전 섹션에서 언급했듯이, HBr만이 고려되며 물 분자는 고려되지 않습니다. 분자량이 화학식 Br-H3O+ 대략 99g / mol의 값을 가질 것이다.
외관
무색 또는 담황색 액체로서 용존 HBr의 농도에 의존한다. 노란색이 많을수록 더 집중되고 위험 할 수 있습니다..
냄새
자극적, 자극적.
악취 문턱
6.67 mg / m3.
밀도
1.49 g / cm3 (수용액 48 % w / w). 이 값은 녹는 점과 끓는 점에 해당하는 값과 마찬가지로 물에 용해 된 HBr의 양에 따라 달라집니다.
융점
-11ºC (12ºF, 393ºK) (49 % w / w 수용액).
끓는점
700 mmHg (수용액 47-49 % w / w)에서 122 ℃ (252 ℉ 393 ℉).
물에 대한 용해도
-221 g / 100 ml (0 ºC에서).
-204 g / 100 ml (15 ºC).
-130 g / 100 ml (100 ºC).
이 값은 브롬화 수소산이 아니라 가스 HBr을 나타냅니다. 알 수 있듯이, 온도를 증가 시키면 HBr의 용해도가 감소한다. 가스에서 자연스러운 행동. 결과적으로, 농축 된 HBr (ac) 용액이 요구된다면 저온에서 작업하는 것이 좋습니다.
고온에서 작업하는 경우, HBr은 가스상의 이원자 분자 형태로 배출되므로 누출을 방지하기 위해 반응기를 밀봉해야합니다.
증기 밀도
2.71 (공기와 관련하여 = 1).
산도 pKa
-9.0. 이렇게 부정적인 상수는 산도의 큰 힘을 나타냅니다..
열량 용량
29.1kJ / mol.
표준 몰 엔탈피
198.7 kJ / mol (298 ºK).
표준 몰 엔트로피
-36.3 kJ / mol.
점화 점
인화성이 없음.
명명법
'브롬 산 브롬 산'이라는 이름은 물의 존재와 브롬의 화합물의 원자가가 -1이라는 두 가지 사실을 결합합니다. 영어로 그것은 다소 더 분명하다 : 브롬화 수소 산, 접두사 '수력'(또는 수력)은 물을 의미한다; 실제로, 그것은 또한 수소를 의미 할 수있다..
브롬은 전기 음성도가 적은 수소 원자에 결합되어 있기 때문에 원자가가 -1입니다. 산소 원자와 연결되거나 상호 작용하는 경우에는 +2, +3, +5 및 +7과 같은 여러가 지 값을 가질 수 있습니다. H는 단 하나의 원자가를 채택 할 수 있기 때문에 접미사 -ico가 그 이름에 추가되는 이유가 여기에 있습니다.
HBr (g), 브롬화 수소는 무수물이며; 즉 물이 없습니다. 그러므로, 그것은 다른 명명법 기준에 따라 명명되며, 할로겐화 수소.
어떻게 형성 되는가??
브롬화 수소산을 합성하는 몇 가지 합성 방법이 있습니다. 그들 중 일부는 다음과 같습니다 :
수소와 브롬의 물 혼합
기술 세부 사항을 기술하지 않고,이 산은 물로 채워진 반응기에서 수소와 브롬의 직접 혼합물로부터 얻을 수있다.
H2 + Br2 => HBr
이런 식으로 HBr이 형성되면서 물에 용해됩니다. 이렇게하면 증류로 끌어 당길 수 있으므로 용액을 다른 농도로 추출 할 수 있습니다. 수소는 가스이고 브롬은 어두운 붉은 액체.
삼 브롬화 인
보다 정교한 과정에서 모래, 수화 된 적린과 브롬이 혼합됩니다. 워터 트랩은 HBr이 탈지하여 대신에 브롬화 수소산을 형성하지 못하도록 얼음 욕조에 놓습니다. 반응은 다음과 같습니다.
2P + 3Br2 => 2PBr3
PBr3 + 3H2O => 3HBr + H3PO3
이산화황 및 브롬
그것을 준비하는 또 다른 방법은 브롬을 물 속의 이산화황과 반응시키는 것입니다.
Br2 + 그래서2 + 2H2O => 2HBr + H2그래서4
이것은 산화 환원 반응입니다. The Br2 그것은 수소와 결합함으로써 전자를 얻는다. 반면에 SO2 황산에서와 같이 다른 산화제와 더 공유 결합을 형성 할 때 산화되고 전자를 잃는다..
용도
브롬화물의 제조
브롬화물 염은 HBr (ac)을 금속 수산화물과 반응 시키면 제조 될 수있다. 예를 들어, 브롬화 칼슘의 생산이 고려됩니다 :
Ca (OH)2 + 2HBr => CaBr2 + H2O
또 다른 예는 브롬화 나트륨입니다 :
NaOH + HBr => NaBr + H2O
따라서, 많은 무기 브롬화물을 제조 할 수있다.
알킬 할라이드의 합성
그리고 유기 브롬화물은 어떻습니까? 이들은 유기 브롬 화합물 : RBr 또는 ArBr.
알콜의 탈수
이들을 얻기위한 원료는 알콜 일 수있다. HBr의 산성도에 의해 양성자 화 될 때, 이들은 물을 형성하는데, 이것은 좋은 방출 그룹이고, 대신 Br의 부피가 큰 원자가 결합되어 탄소와 공유 결합하게 될 것이다 :
ROH + HBr => RBr + H2O
이 탈수는 R-OH 결합의 파열을 촉진하기 위해 100 ℃ 이상의 온도에서 수행됩니다2+.
알켄 및 알킨에 첨가
HBr 분자는 수용액으로부터 알켄 또는 알킨의 이중 또는 삼중 결합에 첨가 될 수있다 :
R2C = CR2 + HBr => RHC-CRBr
RC≡CR + HBr => RHC = CRBr
몇 가지 제품을 얻을 수 있지만 단순한 조건 하에서 브롬이 2 차, 3 차 또는 4 차 탄소 (Markovnikov rule).
이들 할로겐화물은 다른 유기 화합물의 합성에 개입하며, 그 사용 범위는 매우 광범위하다. 또한 이들 중 일부는 신약의 합성 또는 디자인에도 사용될 수 있습니다.
미묘한 clivage
에테르로부터 2 개의 알킬 할라이드가 동시에 수득 될 수 있으며, 각각은 초기 에테르 R-O-R '의 2 개의 측쇄 R 또는 R'중 하나를 운반한다. 알코올의 탈수 반응과 비슷한 일이 있지만 반응 메커니즘은 다릅니다.
반응은 다음의 화학 반응식으로 도식화 될 수있다 :
ROR '+ 2HBr => RBr + R'Br
그리고 물도 방출됩니다..
촉매
그 산도는 효과적인 산 촉매로서 사용될 수있는 정도이다. Br 음이온을 첨가하는 대신- 분자 구조에, 다른 분자가 그것을하기위한 길을 열어 준다..
참고 문헌
- Graham Solomons T.W., Craig B. Fryhle. (2011). 유기 화학. 아민 (10일 판.). 와일리 플러스.
- Carey F. (2008). 유기 화학 (여섯 번째 판). Mc Graw Hill.
- Steven A. Hardinger. (2017). 유기 화학 용어 설명 : 브롬 산. 원본 주소 'chem.ucla.edu'
- 위키 백과. (2018). 브롬 산. 원본 주소 'en.wikipedia.org'
- PubChem. (2018). 브롬 산. 원본 주소 'pubchem.ncbi.nlm.nih.gov'
- 국립 안전 위생 연구소. (2011). 브롬화 수소 [PDF] 원본 주소 'insht.es'
- PrepChem. (2016). 브롬화 수소산의 제조. 원본 주소 : prepchem.com


