발열 반응 공정, 유형 및 예
그 발열 반응 주로 열 또는 빛 방출의 형태로 에너지 전달이 일어나는 일종의 화학 반응입니다. 이름은 그리스어 접두사에서 유래합니다. 엑소, "해외"를 의미한다. 및 열 또는 온도를 지칭하는 용어 "열".
고온에서 기체 상에있는 물질이 팽창 될 때 여기서, 발열 반응은 운동 소닉 에너지를 전달하는 방법을 폭발과 마찬가지로 생성되는 중간에 다른 형태의 에너지를 전송하고있다 맹렬하게.
마찬가지로, 배터리를 사용하는 경우에는 발열 반응을 일으키고,이 경우에만 전기 에너지가 운반됩니다.
색인
- 1 프로세스
- 2 가지 유형
- 2.1 연소 반응
- 2.2 중화 반응
- 2.3 산화 반응
- 2.4 흰개미 반응
- 2.5 반응 중합
- 2.6 핵분열 반응
- 2.7 기타 반응
- 3 예
- 4 참고
프로세스
이전에, 발열 반응이 발생하면 에너지 방출이 발생하고 다음 방정식에서보다 쉽게 시각화 될 수 있다고 언급되었습니다 :
시약 → 제품 (들) + 에너지
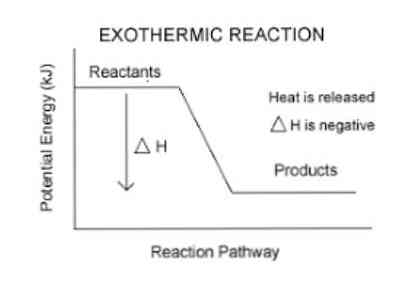
따라서 시스템에 의해 흡수되거나 방출되는 에너지를 정량화하기 위해 엔탈피 ( "H"로 표시)라는 열역학적 파라미터가 사용됩니다. 시스템 (이 경우 화학 반응)에서 주변으로의 에너지 방출이있는 경우, 엔탈피 (ΔH로 표시)의 변화는 음의 값을 갖게됩니다.
그렇지 않으면이 측정 값의 변화량이 양수이면 주위의 열 흡수를 반영합니다. 또한, 시스템의 엔탈피 변화의 크기는 환경으로 또는 환경으로부터 전달되는 에너지 양의 표현입니다.
ΔH의 크기가 클수록 시스템에서 주변 매체로의 에너지 방출이 커집니다.
이것은 이러한 반응에서 새로운 링크가 생성 될 때 방출되는 순 에너지가 링크의 단편화에 사용 된 순 에너지보다 크기 때문입니다.
위의에서이 반응이 클래스는 반응 생성물이 링크에 저장된 에너지의 양을 가지고 있기 때문에 그 처음에 반응물에 포함되는 것보다 더 큰, 매우 일반적인 것을 추론 할 수있다.
유형
실험실 이건 산업 이건 관계없이 화학의 다양한 분야에서 다양한 종류의 발열 반응이 있습니다. 일부는 자발적으로 수행되고 다른 것들은 생산 될 촉매와 같은 특정 조건 또는 물질의 유형을 필요로한다.
다음은 가장 중요한 발열 반응 유형입니다.
연소 반응
연소 반응은 일반적으로 불꽃을 발생하는 광이며 열 에너지, 열 및 광 방출의 결과, 하나 이상의 물질이 산소와 반응 할 때 발생하는 그 산화 환원 유형.
중화 반응
중화 반응은 산성 화학 종과 알칼리성 물질 (염기) 사이의 상호 작용에 의해 발열 성을 나타내는 염과 물을 형성하는 것을 특징으로한다.
산화 반응
탄화수소의 산화에서 발생하는 것처럼 산소의 산화는 많은 양의 에너지를 방출하기 때문에 발열 반응을 보이는이 유형의 많은 반응이 있습니다..
흰개미 반응
이 반응은 약 3000 ℃의 온도를 생성 할 수 있으며, 많은 금속 산화물과 알루미늄 분말의 높은 친 화성으로 인해 강철과 철의 용접에 사용됩니다.
중합 반응
이러한 유형의 반응은 그 고분자 중합체라는 구조를 형성하는 체인으로 결합 된 반복 단위가 단량체라는 화학 종의 수의 반응시 발생.
핵분열 반응
이 과정은 질량이 큰 것으로 간주되는 원자핵 (즉, 200보다 큰 질량수)의 핵을 나누어 중간 크기의 작은 크기의 단편 또는 핵을 생성하는 것을 의미합니다.
하나 이상의 중성자가 형성되는이 반응에서, 더 큰 무게의 코어는 그 제품보다 낮은 안정성을 갖기 때문에 많은 양의 에너지가 방출된다.
기타 반응
황산과 반응하여 그러한 어떤 탄수화물 탈수 다른 관련성이 발열 반응은, 물을 갖는 수산화 나트륨 흡수 야외 노출되거나 많은 부식 반응에서 금속 종의 산화가있다.
예제들
아래는 위에서 언급 한 것처럼 에너지를 방출한다는 사실 때문에 음의 값을 갖는 엔탈피의 변화를 생성하는 발열 반응의 몇 가지 예입니다..
예를 들어, 프로판의 연소는 자연 발열 반응이다.
C3H8(g) +5O2(g) → 3CO2(g) + 4H2O (l)
발열 반응의 또 다른 경우는 탄산나트륨과 염산 사이의 중화 반응으로 나타납니다.
NaHCO3(ac) + HCl (ac) → NaCl (ac) + H2O (1) + CO2(g)
호흡기에 사용 된 에탄올의 아세트산으로의 산화 반응 또한 제시되며, 그의 반응은 다음 식과 같다.
3CH3CH2OH + 2K2크롬2O7 + 8H2그래서4 → CH3COOH + 2Cr (SO4)3 + 2K2그래서4 + 11H2O
발열 반응의 다른 부류는 소위 테르밋 반응 (thermite reaction)으로, 아래에 예시 된 바와 같이 알루미늄이 금속 산화물과 결합되어있다 :
2Al (s) + 믿음2O3(들) → 알2O3(s) + Fe (l)
위에서 설명한 예 이외에도 퇴비화를위한 특정 유기 폐기물의 분해와 같이 발열로 간주되는 다양한 반응이 있습니다..
또한, 다른 반응 중 특성 반딧불 생물 발광, 심지어 호흡을 생산하는 루시퍼 라제 효소의 작용에 의해 안료 산화 루시페린 강조.
참고 문헌
- 위키 백과. (s.f.). 발열 반응. es.wikipedia.org에서 검색 됨
- BBC (s.f.). 에너지 변화와 가역적 인 반응. bbc.co.uk에서 가져옴
- Chang, R. (2007). 화학, 9 판. (맥그로 힐).
- Walker, D. (2007). 화학 반응. books.google.co.ve에서 가져옴
- Saunders, N. (2007). 화학 반응 탐구. books.google.co.ve에서 가져옴


