칼슘 인산염 (Ca3 (PO4) 2) 구조, 재산, 대형 및 용도
그 인산 칼슘 화학식이 Ca 인 무기 및 제 3 염3(PO4)2. 이 공식에 따르면이 소금의 조성은 칼슘과 인산염 각각 3 : 2입니다. 이것은 Ca 양이온이 보여지는 더 낮은 이미지에서 직접 볼 수 있습니다.2+ 및 음이온 PO43-. 매 3 년마다2+ 2 개의 PO43- 그들과 상호 작용하기.
한편, 인산 칼슘은 수화 및 pH의 정도뿐만 아니라 Ca / P 비율에 따라 달라지는 일련의 염을 의미합니다. 사실, 존재할 수 있고 합성 될 수있는 많은 유형의 인산 칼슘이 있습니다. 그러나, 말 그대로 명명법 다음에, 인산 칼슘은 삼염화 칼슘,.

Ca를 포함한 모든 칼슘 인산염3(PO4)2, 그들은 단색의 흰색이고 약간 회색 빛을 띤다. 입자는 미세하고 미세하며 결정질 일 수 있으며 입자 크기는 마이크로 미터 정도입니다. 심지어 이들 인산염의 나노 입자가 제조되어 뼈에 대한 생체 적합성 물질이 설계되었습니다.
이 생체 적합성은 이러한 염이 치아에서 발견되고, 간단히 말해서 포유 동물의 뼈 조직에서 발견된다는 사실에 기인합니다. 예를 들어, hydroxyapatite는 결정질 인산 칼슘이며, 동일한 인산염의 비정질 상과 상호 작용합니다.
이것은 비정질 및 결정질 인산 칼슘이 존재 함을 의미합니다. 이러한 이유로 인산 칼슘을 기본으로 한 물질을 합성 할 때 다양성과 다양한 옵션이 놀라운 것은 아닙니다. 연구원들이 매일 세계에 관심을 갖고있는 재료들은 뼈의 복원에 초점을 맞추고있다..
색인
- 1 인산 칼슘의 구조
- 1.1 비정질 인산 칼슘
- 1.2 나머지 가족
- 2 물리 화학적 특성
- 2.1 이름
- 2.2 분자량
- 2.3 물리적 설명
- 2.4 맛
- 2.5 융점
- 2.6 용해도
- 2.7 밀도
- 2.8 굴절률
- 2.9 표준 엔탈피 훈련
- 2.10 보관 온도
- 2.11 pH
- 3 교육
- 3.1 질산 칼슘과 인산 수소 암모늄
- 3.2 수산화칼슘과 인산
- 4 용도
- 4.1 뼈 조직에서
- 4.2 Bioceramic 시멘트
- 4.3 의사
- 4.4 기타
- 5 참고
인산 칼슘의 구조
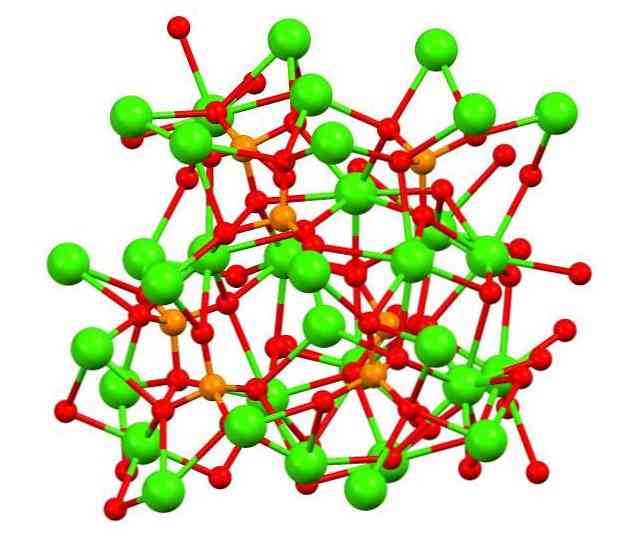
위 이미지는 불순물로서 마그네슘과 철을 함유하고있을 수있는 이상한 휘 틀록 나무 광물에서 삼차 계 옥양 제 인산염의 구조를 보여준다.
언뜻보기에는 복잡해 보일 수도 있지만, 모델이 인산염의 산소 원자와 칼슘의 금속 중심 사이의 공유 결합을 가정한다는 것을 분명히하는 것이 필요합니다.
그러나 표현의 방법으로는 상호 작용이 정전기 적이라는 것이 타당합니다. 즉, 양이온 Ca2+ PO 음이온에 끌린다.43- (Ca2+- O-PO33-). 이를 염두에두고, 칼슘 (녹색 구체)이 음으로 하전 된 산소 원자 (적색 구체)로 둘러싸인 이유를 이해합니다..
이온이 너무 많으면 대칭 배열이나 패턴을 볼 수 없습니다. 칼슘3(PO4)2 저온에서 사용 (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, 영어 약어).
한편, 고온에서, 이는 다 형체 α-Ca3(PO4)2 (α-TCP)로 구성되며, 단위 격자는 단사 결정계에 해당한다. 더 높은 온도에서, 다 형체 α'-Ca는 또한 형성 될 수있다3(PO4)2, 육방 정계 결정 구조.
비정질 인산 칼슘
소금으로부터 예상되는 인산 칼슘의 결정 구조가 언급되었습니다. 그러나 그것은 엄격한 의미의 결정보다는 "인산 칼슘 유리"의 유형과 더 관련이있는 무질서하고 비대칭적인 구조를 나타낼 수 있습니다.
이것이 일어날 때, 인산 칼슘은 비정질 구조 (ACP, 비정질 인산 칼슘). 몇몇 저자들은 Ca의 생물학적 특성을 담당하는 구조의이 유형을 지적한다3(PO4)2 뼈 조직에서 그 수리 및 생체 측정이 가능하다..
핵 자기 공명 (NMR)에 의한 구조의 해명을 통해, OH 이온의 존재가 발견되었습니다- 및 HPO42- ACP에서. 이들 이온은 인산염 중 하나의 가수 분해에 의해 형성됩니다 :
PO43- + H2O <=> HPO42- + OH-
결과적으로, ACP의 진정한 구조는 더욱 복잡해지며, 그 이온의 조성은 다음 공식으로 표현됩니다 : Ca9(PO4)6-x(HPO4)x(OH)x. 'x'는 수화도를 나타냅니다. x = 1이면 수식은 다음과 같습니다. Ca9(PO4)5(HPO4) (OH).
PCA가 가질 수있는 다른 구조는 Ca / P 몰비에 달려있다. 즉, 칼슘과 인산염의 상대적인 양은 모든 결과 구성을 바꾼다..
나머지 가족
인산 칼슘은 실제로 무기 화합물의 계열이며, 차례로 유기 매트릭스와 상호 작용할 수 있습니다.
다른 인산염은 칼슘을 동반하는 음이온을 변화시킴으로써 간단히 얻어진다 (PO43-, HPO42-, H2PO4-, OH-)뿐만 아니라 고체의 불순물 유형. 따라서 11 개까지의 인산 칼슘 또는 그 이상은 각각 자체 구조 및 특성을 가지고 자연적으로 또는 인위적으로 생길 수 있습니다..
아래는 일부 인산염과 그 각각의 구조와 화학 구조식입니다 :
-수소 인산 칼슘 이수화 물, CaHPO4∙ 하반기2O : 단조.
-칼슘 디 히드로 겐 포스페이트 일 수화물, Ca (H)2PO4)2∙ H2오 : triclinic.
-무수 이산 인산염, Ca (H)2PO4)2: 삼엽기.
-Ocalcium hydrogen phosphate (OCP), Ca8H2(PO4)6: 삼엽기 그것은 hydroxyapatite의 합성에서 전구체이다..
-수산화 인회석, Ca5(PO4)3OH : 육각형.
물리 화학적 특성
이름
-인산 칼슘
-인산 칼슘
-Tricalcium diphosphate
분자량
310.74 g / 몰.
물리적 설명
그것은 무취의 흰색 고체이다..
맛
맛없는.
융점
1670 ºK (1391 ºC).
용해도
-물에 실질적으로 녹지 않는다..
-에탄올에 불용성.
-묽은 염산 및 질산에 가용성.
밀도
3.14 g / cm3.
굴절률
1,629
표준 엔탈피 훈련
4126 kcal / mol.
보관 온도
2 ~ 8ºC.
pH
인산 칼슘 50 g / L.
교육
질산 칼슘과 인산 수소 암모늄
인산 칼슘을 생산하거나 형성하는 수많은 방법이 있습니다. 그 중 하나는 두 가지 염, Ca (NO)3)2∙ 4H2O 및 (NH4)2HPO4, 이전에 각각 절대 알코올 및 물에 용해되었다. 하나의 소금은 칼슘을 제공하고 다른 하나의 인산염.
이 혼합물로부터 ACP 침전물을 얻은 다음 800 ℃ 오븐에서 2 시간 동안 가열한다. 이 과정의 결과로, β-Ca가 얻어진다3(PO4)2. 신중하게 온도, 교반 및 접촉 시간을 조절함으로써 나노 결정 형성이 일어날 수있다..
다 형체 α-Ca3(PO4)2 인산염을 1000 ℃ 이상으로 가열 할 필요가있다. 이 가열은이 다 형체를 실온에서 사용하기에 충분히 안정화시키는 다른 금속 이온의 존재 하에서 수행된다; 즉, 안정적인 메타 상태로 유지됩니다..
수산화칼슘과 인산
인산 칼슘은 또한 수산화칼슘과 인산의 용액을 혼합하여 산 - 염기 중성화를 일으킴으로써 형성 될 수있다. 모액에서 숙성시키고 여과, 세척, 건조 및 체질을 수행하는 반나절 후, 비정질 인산염의 과립 분말 ACP.
이 ACP 반응 생성물은 다음 화학 방정식에 따라 변형됩니다.
2Ca9(HPO4) (PO4)5(OH) => 2Ca9(P2O7)0.5(PO4)5(OH) + H2O (T = 446.60 ℃)
2Ca9(P2O7)0.5(PO4)5(OH) => 3Ca3(PO4)2 + 0.5H2O (T = 748.56 ° C에서)
이러한 방식으로, β-Ca가 얻어진다3(PO4)2, 가장 흔하고 안정한 다 형체.
용도
뼈 조직
칼슘3(PO4)2 그것은 뼈 가루의 주요 무기질 성분입니다. 그것은 뼈에있는 미네랄과의 화학적 유사성으로 설명되는 뼈 대체 이식의 구성 요소입니다.
칼슘 인산염 생체 재료는 뼈 결함을 교정하고 티타늄 금속 보철물을 코팅하는 데 사용됩니다. 인산 칼슘은 그 (것)들에 입금되고, 환경에서 그들을 고립시키고 티타늄 부식 과정을 감속합니다.
칼슘 인산염, 칼슘3(PO4)2, 세라믹 재료 생산에 사용됩니다. 이 물질들은 생체 적합성이 있으며 현재 치주 질환, 근관 치료 및 기타 조건으로 인한 치조골 손실을 복구하는 데 사용됩니다..
그러나 만성 박테리아 감염이없는 지역에서 치근단 뼈 복구를 촉진하기 위해서만 사용해야합니다.
자가 인 뼈 이식편을 사용할 수없는 경우 인산 칼슘을 골 결손의 치료에 사용할 수 있습니다. 단독으로 또는 폴리 글리콜 산과 같은 생분해 성 및 흡수성 중합체와 함께 사용하는 것이 가능하다.
바이오 세라믹 시멘트
인산 칼슘 시멘트 (CPC)는 뼈 조직의 수리에 사용되는 또 다른 bioceramic입니다. 그것은 여러 유형의 인산 칼슘 분말을 물과 혼합하여 페이스트를 형성함으로써 만들어집니다. 페이스트는 뼈의 결함이나 구멍에 주사되거나 조절 될 수 있습니다..
시멘트가 성형되고 점차 재 흡수되어 새로 형성된 뼈로 대체됩니다..
의사들
-칼슘3(PO4)2 그것은 기본 소금이므로 과도한 위산을 중화시키고 pH를 증가시키는 제산제로 사용됩니다. 치약에서는 치아와 뼈의 지혈 재의 과정을 촉진하기 위해 칼슘과 인산염의 공급원을 제공합니다.
-칼슘을 대체하는 가장 저렴한 방법은 탄산염과 시트르산을 사용하는 것이지만, 영양 보충제로도 사용됩니다..
-인산 칼슘은 테타 니 (tetany), 잠재적 인 저칼슘 혈증 및 유지 요법의 치료에 사용될 수 있습니다. 또한 임신 및 수유 기간 동안 칼슘 보급에 유용합니다..
-방사성 동위 원소 인 방사성 물질 (Ra-226)과 스트론튬 (Sr-90)의 오염 처리에 사용됩니다. 인산 칼슘은 소화관에서 방사성 동위 원소의 흡수를 차단하여 이로 인한 피해를 제한합니다.
기타
-인산 칼슘은 새의 사료로 사용됩니다. 또한, 그것은 치석을 제어하는 치약에 사용됩니다.
-그것은 예를 들어 테이블 소금이 압축되는 것을 방지하기 위해 고결 방지제로 사용됩니다..
-그것은 밀가루에 대한 표백제로 작동합니다. 반면, 돼지의 돼지에서 바람직하지 않은 착색을 방지하고 튀김의 상태를 개선하는 동안.
참고 문헌
- Tung M.S. (1998) 칼슘 인산염 : 구조, 조성, 용해도 및 안정성. 에서 : Amjad Z. (eds) 칼슘 인산염 생물학과 산업 시스템. Springer, Boston, MA.
- Chang Xu, Suchun Yu, Xiaopei Wu, Honglian Dai 등이있다. (2018). "나노 β-Tricalcium 인산염의 합성, 특성화 및 Hepatocellular 암종 세포에 대한 억제,"Journal of Nanomaterials, vol. 2018 년, 기사 ID 7083416, 7 페이지, 2018.
- Combes, 그리스도와 레이, 기독교. (2010). 무정형 인산 칼슘 : 생체 물질의 합성, 특성 및 용도. Acta Biomaterialia, vol. 6 (n ° 9). pp. 3362-3378. ISSN 1742-7061
- 위키 백과. (2019). Tricalcium 인산염. 원본 주소 'en.wikipedia.org'
- Abida et al. (2017). Tricalcium 인산 분말 : 준비, 특성 및 압축 능력. Mediterranean Journal of Chemistry 2017, 6 (3), 71-76.
- PubChem. (2019). 인산 칼슘. 원본 주소 'pubchem.ncbi.nlm.nih.gov'
- Elsevier (2019). 인산 칼슘. 과학 직접. 원본 주소 'sciencedirect.com'


