유기 화합물과 무기 화합물의 차이점
그 유기 화합물과 무기 화합물의 주된 차이점 탄소 원자의 존재.
유기 화합물은 탄소 원자를 함유하며, 보통 탄화수소를 형성하는 수소 원자를 갖는다. 그 부분을 위해, 거의 모든 무기 화합물은 탄소 및 / 또는 수소 원자를 함유하지 않는다..
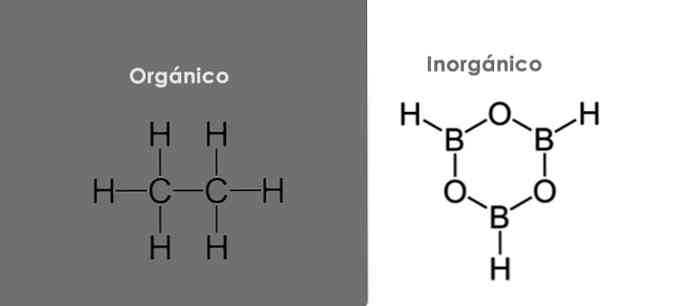
유기 화합물과 무기 화합물의 주된 차이점
대부분의 무기 화합물에는 탄소가 포함되어 있지 않지만 몇 가지 예외가 있습니다. 예를 들어, 일산화탄소와 이산화탄소는 탄소 원자.
그러나, 그 양은 분자 내에 존재하는 산소와 강한 결합을 형성하기에 충분하지 않다. 이 때문에 과학자들은 항상 이러한 화합물을 무기로 간주했습니다. 따라서 화합물에 석탄이 포함되어 있어도 반드시 유기물로 간주되는 것은 아닙니다..
두 화합물의 또 다른 큰 차이점은 분자의 유형과 살아있는 존재와의 관련성입니다. 유기 화합물은 DNA, 지질, 당, 지질 산에서 발견되는 핵산과 같은 것들을 포함합니다. 생물의 세포에서 발견되는 단백질이나 효소는 세포 과정에 필요합니다. 탄화수소 연료 또한 유기 연료로 간주됩니다..
무기 화합물은 염분, 금속 및 기타 필수 구성 요소와 같은 요소를 포함합니다. 단독 원소로 만들어진 물질과 수소 원자와 결합 된 탄소 원자가없는 화합물은 모두 무기로 간주됩니다.
이러한 특성에도 불구하고 유기 화학자는 유기 화합물과 무기 화합물의 차이점에 대한 최종 합의에 도달하지 못했습니다. 논쟁이 아직 끝나지 않았기 때문에 가장 인정 된 확인 방법으로 분자 내 탄소의 존재를 언급합니다.
유기 화합물
이들 화합물에서, 하나 이상의 탄소 원자는 다른 원소의 원자에 결합되어있다. 이들이 부착되는 가장 일반적인 요소는 대개 수소, 산소 및 질소입니다. 탄소를 함유하고 유기물로 간주되지 않는 화합물은 시안화물, 탄산염 및 탄화물입니다..
모든 알려진 생명체는 유기 화합물을 기반으로하기 때문에 전통적으로 유기 화합물이 매우 중요합니다. 가장 기본적인 석유 화학 제품은 유기 화학의 기초로 간주됩니다..
유기 화합물의 현대적인 정의는 상당량의 탄소를 함유하고있는 화합물입니다. 오늘날 알려진 많은 유기 화합물은 살아있는 유기체에서 발견 된 어떤 물질과도 관련이 없지만.
수소와 탄소의 결합이 없더라도 유기 화합물로 간주되는 몇 가지 화합물이 있습니다. 이들은 벤젠 엑스솔, 메독 살산 및 사염화탄소를 포함한다.
유기 화합물은 천연 화합물과 합성 화합물로 분류 할 수있다..
천연 화합물
식물과 동물에 의해 생성 된 화합물을 지칭합니다. 이들 화합물 중 많은 것들은 인위적으로 제조하는 것이 매우 비싸기 때문에 천연 원료로부터 추출됩니다.
가장 흔한 것은 설탕, 비타민 B12와 같은 일부 알칼로이드와 영양소입니다. 일반적으로 그들은 크거나 복잡한 분자를 가지고 있으며 생물에서 합리적인 양으로 발견 될 수있는 모든 화합물입니다.
합성 화합물
다른 화합물의 반응에 의해 제조 된 화합물은 합성으로 간주된다. 그들은 자연에서 발견되는 화합물이거나 자연적으로 발생하지 않는 화합물 일 수 있습니다.
플라스틱 및 고무와 같은 대부분의 폴리머는 반 합성 유기 화합물입니다..
생명 공학
에탄올이나 인슐린과 같은 많은 유기 화합물은 박테리아와 효모의 유기체를 사용하여 산업적으로 제조됩니다. 일반적으로 유기체의 DNA는 신체에서 정상적으로 생성되지 않는 화합물을 발현하도록 변형됩니다.
생명 공학에 의해 만들어진 많은 화합물은 이전에는 자연에 존재하지 않았다..
무기 화합물
화학에서 C-H 루프라고하는 탄소와 수소 사이의 결합을 포함하지 않는 화합물은 무기로 간주 될 수 있습니다. 또한, 무기 화합물은 지질 학적으로 미네랄이거나 수소 분자에 붙어있는 탄소를 포함하지 않는 화합물 인 경향이있다. 이것이 많은 무기 화합물이 금속.
화합물이 다음 기준 중 하나를 충족하는 경우 무기 화합물로 간주 될 수 있습니다.
- 석탄이 조성되어 있지 않다..
- 비 생물학적 기원이다..
- 그것은 생물체에서 발견되거나 통합 될 수 없다..
현재, 무기 화합물은 또한 유기 성질이 아닌 임의의 화합물로 정의 될 수있다.
이러한 이유로 탄소를 함유 한 간단한 화합물을 무기물이라고합니다. 이들 화합물 중 일부는 일산화탄소, 이산화탄소, 중탄산 나트륨, 탄화물, 탄산염 및 시아 나이드를 포함합니다..
이 화합물들 중 많은 것들이 유기체를 포함한 많은 유기체 시스템의 정상적인 부분입니다. 이것은 화학 물질이 무기로 기술 될 수 있음을 의미하지만 이것이 생물체에 존재하지 않는다는 것을 의미하지는 않습니다.
미네랄은 주로 산화물과 황산염이며, 생물학적 기원이지만 엄격하게 무기질입니다. 사실, 지구의 대부분은 무기입니다.
지구의 층 구성 요소가 잘 설명되어 있지만, mineralization 과정과 깊은 층의 구성은 조사에서 활성 영역으로 남아 있습니다.
진실은 우주에있는 대부분의 화합물이 자연적으로 무기라는 사실입니다. 이러한 이유로 무기 화합물은 일상 생활에서 많은 응용과 실용을 가지고 있습니다. 세계에서 많은 화합물이 무기이기 때문에,이 화합물은 많은 다른 형태를 가질 수 있으며 매우 다른 특성을 가질 수 있습니다.
예를 들어 많은 것은 금속이므로 전기를 전송할 수 있습니다. 그들은 또한 매우 뚜렷하고 밝은 색상뿐만 아니라 높은 끓는점을 갖는 경향이 있습니다. 일반적으로 물에 잘 용해되며 많은 물질이 결정을 형성 할 수 있습니다..
참고 문헌
- 유기 대 Compunds 유기. 부드러운 학교. softschools.com에서 회복.
- 유기와 무기의 차이점은 무엇입니까? (2016) 과학. thoughtco.com에서 가져온.
- 유기 화합물. 화학 화합물. Britannica 백과 사전. britannica.com에서 회복.
- 미국의 연료 및 석유 화학 제조 업체. (2016). afpm.org에서 회복.
- Geomicrobiology : 어떻게 분자 과학 상호 작용이 생화학 시스템을 뒷받침하는지. (2002). 과학 -296. sciencemag.org에서 검색 함.
- 무기 화합물은 무엇입니까? 정의, 특성 및 예. 제 20과, 제 4 장..


